
【题目】富氧燃烧技术中,用氧气含量高于21%的富氧空气支持燃烧,能起到节能和减少碳排放的作用。富氧燃烧的产物中CO2 的含量可达到95%,有助于CO2回收利用。该技术的主要流程如下:
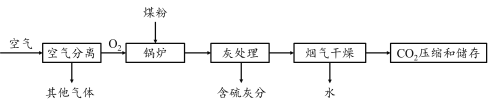
(1)空气分离的过程中发生的是物理变化,图中其它气体的主要成分是________。
(2)该流程中涉及的物质中,属于氧化物的是________(写出一种即可)。
(3)根据信息推测,煤粉中含有的主要元素有________(填字母序号)。
A碳元素 B铁元素 C硫元素 D钠元素
(4)关于富氧燃烧技术,下列说法不合理的是________(填字母序号)。
A与普通燃烧相比,富氧燃烧锅炉中煤粉的燃烧更剧烈
B煤粉燃烧更充分,可以节约燃料,达到节能减排的目的
CCO2无毒,压缩和存储的CO2直接排放到空气中
【答案】氮气(有氮气即可) CO2(或H2O) AC C
【解析】
(1)空气中主要含有氧气和氮气,所以空气分离的过程中发生的是物理变化,图中其它气体的主要成分是氮气;
(2)氧化物是由两种元素组成的纯净物,其中一种是氧元素的纯净物,所以该流程中涉及的物质中,属于氧化物的是CO2和H2O;
(3)化学反应前后,元素种类不变,所以煤粉中含有的主要元素有碳、硫,故选:AC;
(4)富氧燃烧技术中,用氧气含量高于21%的富氧空气支持燃烧,能起到节能和减少碳排放的作用,富氧燃烧的产物中CO2的含量可达到95%,有助于CO2回收利用,所以
A 与普通燃烧相比,富氧燃烧锅炉中煤粉的燃烧更剧烈,故正确;
B 煤粉燃烧更充分,可以节约燃料,达到节能减排的目的,故正确;
C CO2无毒,但是会产生温室效应,压缩和存储的CO2不能直接排放到空气中,故错误。
故选:C。
故答案为:(1)氮气(有氮气即可);
(2)CO2(或H2O);
(3)AC;
(4)C。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:初中化学 来源: 题型:
【题目】(7分)FeCl3溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.
写出本实验发生反应的化学方程式 .
Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,如图观察到 ,就可以粗略判断,得出实验结果.

为进一步判断上述实验结论的准确性,运用图,小刚同学进行了如下实验方案设计.
Ⅱ.
[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间.
[方案二]在不同过氧化氢浓度下,测定 ;
方案二的实验测量结果:
| 30% H2O2溶液的体积(mL) | 2% FeCl3溶液的体积(mL) | 加入H2O的体积(mL) | 反应的时间(min) | 生成O2的体积(mL) |
1 | 5 | x | 20 | 5 | V1 |
2 | 10 | 3 | 15 | y | V2 |
表中x= ,y= .
实验结论:通过测量,若V1 V2(填“>”、“=”或“<”),说明 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某粒子的结构示意图为![]() ,回答下列问题。
,回答下列问题。
(1)若该粒子不带电,则x=_____,该粒子的符号为_____。
(2)若该粒子带三个单位正电荷,则x=_____,该粒子的符号为_____。
(3)若该粒子带一个单位负电荷,则x=_____,该粒子的符号为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知石榴皮中含有一种叫做N-甲基异石榴皮碱(C9H17NO)的物质。请根据石榴皮碱的化学式回答下列问题:
(1)该物质由____元素组成,其的一个分子中碳、氢、氮、氧的原子个数比为______________ 。
(2)该物质的相对分子质量是(列出计算式)________________;C、H、N、O的质量比为(列出计算式)_________________。该物质中碳元素的质量分数为_____________(保留两位小数,下同)
(3)1.55g该物质中含有的氢元素的质量为_________________ g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图从A或B两题中任选一个作答,若两题均作答,按A计分。
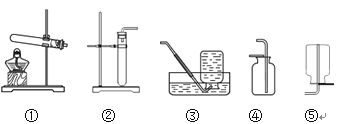
A | B |
(1)实验室用过氧化氢和二氧化锰混合制取氧气的文字表达式为___________。 (2)选用的发生装置为___________(填字母序号,下同)。 (3)请选择一个收集装置___________,并说明该装置可用于收集氧气的理由是____________。 | (1)实验室用高锰酸钾制取氧气的文字表达式为___________。 (2)选用的发生装置为___________(填字母序号,下同)。 (3)请选择一个收集装置___________,并说明该装置可用于收集氧气的理由是____________。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为某同学进行电解水实验的装置图,据此回答:
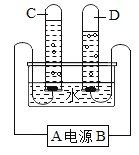
(1)图中A端为电源的____(填“正”或“负”)极;
(2)C试管中收集到的气体是____
(3)为了 __________________________,需要在水中加入稀硫酸或氢氧化钠溶液;
(4)写出该反应的化学方程式:_________________________________________________;
(5)在水的电解实验中,在反应变化前后没有改变的微粒是____。(用化学符号表示)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组测定空气中氧气的体积分数。
(1)根据如图回答问题。
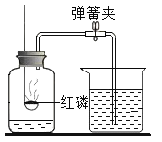
①红磷燃烧的化学方程式为_______________________。
②实验过程中发现实验结果偏大,下列原因正确的是(________________)
A 红磷过量 B 装置气密性不好 C 将燃着的红磷缓慢伸入瓶内
D 未等装置冷却就打开弹簧夹 E 瓶内预先装了少量水
(2)用四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数。反应原理为:2Na2S4+O2+2H2O=8S![]() +4NaOH(氢氧化钠)。小资料:四硫化钠(Na2S4)与氧气、水反应生成难溶于水的固体硫(S)和易溶于水的氢氧化钠。
+4NaOH(氢氧化钠)。小资料:四硫化钠(Na2S4)与氧气、水反应生成难溶于水的固体硫(S)和易溶于水的氢氧化钠。
(实验过程):
①取足量的四硫化钠固体加入试管中,再加入适量的水,迅速塞紧橡胶塞,充分振荡。测量液面至橡胶塞下沿的距离,记录数据h1(如图1所示)。
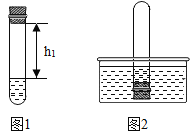
②将该试管插入水中(如图2所示),拔下橡胶塞,观察到_____________________,塞紧橡胶塞。将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2。理论上h2:h1=______。
③按照①和②再重复实验2次、3次实验数据如下表所示.根据第三次实验数据,计算空气中氧气的体积分数为________%(结果精确到0.1%)
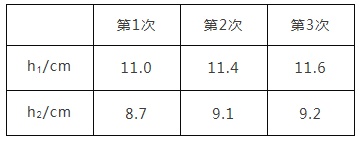
④若该实验中实际消耗的Na2S4质量为10g,则理论上生成的硫的质量为______g(计算结果保留两位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B…H八种物质,有下图所示关系:其中E、F是常见的液体,C是一种黑色固体单质,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变。试推断:

(1)写出物质的名称:B_____;F_____。
(2)写出反应①的的符号表达式:_____。
(3)上述关系中属于化合反应的是_____(填编号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,用“W”型玻璃管进行微型实验。下列有关叙述不正确的是
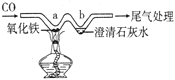
A. a处发生反应的化学方程式是Fe2O3+3CO=2Fe+3CO2
B. b处发生的现象是澄清石灰水变浑浊
C. 此装置可节约用品,污染小,现象明显
D. 尾气用燃着的酒精灯将其点燃,或备用气球收集起来
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com