
某化工集团出售的小苏打样品NaHCO3的质量分数的标注≥95%,某化学兴趣小组的同学对此产生了疑问,进行了下面的实验:向盛有13g小苏打固体样品(所含杂质不溶于水也不与酸反应)的烧杯中,加入100.5g硫酸溶液恰好反应。反应过程用精密仪器测得烧杯连同药品的质量与反应时间的关系如表所示。烧杯连同药品的起始质量为200.0g。反应的化学方程式为:![]()
| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 烧杯及所盛物质的总质量/g | 200.0 | 196.7 | 194.6 | 193.9 | 193.4 | M | 193.4 |
回答下列问题:
(1)该小组因故没有记录反应时间为5min时的数据M。你由表中数据推测M=___________g。
(2)当碳酸氢钠与硫酸溶液完全反应时,所产生二氧化碳的质量为___________g。
(3)该小苏打样品中NaHCO3的质量分数为多少?是否合格?(计算结果精确到0.1%)
(4)求实验结束后溶液中溶质的质量分数?
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
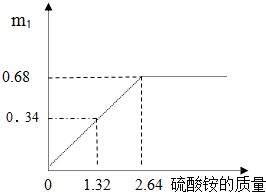 某化工集团生产的化肥硫酸铵[(NH4)2SO4],含有硫酸钾.其产品包装上标明:硫酸铵[(NH4)2SO4]≥70%.为测定该化肥产品中硫酸铵的质量分数,进行如下实验:取一定量的该化肥配成200g溶液,平均分成两份,(假设所有的反应都是完全反应)
某化工集团生产的化肥硫酸铵[(NH4)2SO4],含有硫酸钾.其产品包装上标明:硫酸铵[(NH4)2SO4]≥70%.为测定该化肥产品中硫酸铵的质量分数,进行如下实验:取一定量的该化肥配成200g溶液,平均分成两份,(假设所有的反应都是完全反应)| 加入硝酸钡溶液质量/g | 10 | 20 | 45 | 55 |
| 产生白色沉淀质量/g | 2、33 | 4、66 | 6、99 | 6、99 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某化工集团生产的化肥硫酸铵[(NH4)2SO4],含有硫酸钾.其产品包装上标明:硫酸铵[(NH4)2SO4]≥70%.为测定该化肥产品中硫酸铵的质量分数,进行如下实验:取一定量的该化肥配成200g溶液,平均分成两份,(假设所有的反应都是完全反应)
某化工集团生产的化肥硫酸铵[(NH4)2SO4],含有硫酸钾.其产品包装上标明:硫酸铵[(NH4)2SO4]≥70%.为测定该化肥产品中硫酸铵的质量分数,进行如下实验:取一定量的该化肥配成200g溶液,平均分成两份,(假设所有的反应都是完全反应)| 加入硝酸钡溶液质量/g | 10 | 20 | 45 | 55 |
| 产生白色沉淀质量/g | 2、33 | 4、66 | 6、99 | 6、99 |
查看答案和解析>>
科目:初中化学 来源:2011年广东省佛山市碧江中学中考化学模拟试卷(八)(解析版) 题型:解答题
| 加入硝酸钡溶液质量/g | 10 | 20 | 45 | 55 |
| 产生白色沉淀质量/g | 2、33 | 4、66 | 6、99 | 6、99 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com