
����Ŀ����Դ��������������ͷ�չ���ɻ�ȱ�����ء�
��1��Ϊ��������β���Կ�������Ⱦ����Ȼ���ѳ��Դ���������Ϊ������ȼ�ϡ���Ȼ����Ҫ�ɷ��Ǽ��飬д������ȼ�յĻ�ѧ����ʽ_____��
��2�����б仯�����У�������ѧ�仯�����¶����ߵ���_____������ĸ����
Aľ̿ȼ�� Bϡ��Ũ���� C�����Ʒ���ˮ�� Dþ������ϡ���� Eľ̿�������̼��Ӧ F����粒������ˮ��
��3��һ�������£���һ���ܱ������ڷ���ij��Ӧ����÷�Ӧǰ������ʵ�������ͼ��ʾ��
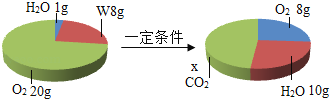
����˵����ȷ����_____������ĸ����
A X��ֵΪ11
B �÷�Ӧ�����û���Ӧ
C ����W������Ԫ�����
D W��̼����Ԫ��ԭ�Ӹ�����Ϊ1��4
��4��Ǧ������ŵ��ȶ�����۽ϵ͵��ŵ��Ӧ�ù㷺��������Ҫ�õ�������������Ϊ28%��������Һ��ʵ������98%��Ũ���ᣨ�ܶ�1.84g/mL������28%��������Һ1000g����Ҫ98%Ũ��������Ϊ___mL��������������0.1����
���𰸡�CH4+2O2![]() CO2+2H2O ACD ACD 155.3
CO2+2H2O ACD ACD 155.3
��������
��1����Ȼ����Ҫ�ɷ��Ǽ��飬����ȼ�������˶�����̼��ˮ����Ӧ�Ļ�ѧ����ʽ��CH4+2O2![]() CO2+2H2O��
CO2+2H2O��
��2��ľ̿ȼ�ա������Ʒ���ˮ�С�þ������ϡ���ᣬ���ϱ仯�������˻�ѧ�仯�����¶����ߣ�ϡ��Ũ������Һ�¶�����û�з�����ѧ�仯��ľ̿�������̼��Ӧ�������ȷ�Ӧ������粒������ˮ�У���Һ�¶Ƚ��͡�
��3����������������W������������С�������Ƿ�Ӧ��ҷ�Ӧ�����������8g+��20g��8g����20g����ˮ���������ӣ�������ֵ��10g��1g��9g�����������غ㶨�ɲμӻ�ѧ��Ӧ�ĸ����������ܺ͵��ڷ�Ӧ�����ɵĸ����������ܺͣ����Զ�����̼���������������ɵ�������20g��9g��11g���˷�Ӧ�ı���ʽ�ɱ�ʾΪW+O2��CO2+H2O��
A�������Ϸ�����֪��X��ֵΪ11����ȷ��
B���÷�Ӧ�������������ֻ���������û���Ӧ������ȷ��
C�����������غ㶨�ɣ��ɷ�Ӧ����ʽ���Կ���W��һ������̼������Ԫ�أ��Ƿ�����Ԫ����Ҫͨ���������е���Ԫ���뷴Ӧ�������������бȽϣ����ɵ�ˮ����Ԫ�ص�����Ϊ��9g��![]() ��8g��������̼����Ԫ�ص�������11g��
��8g��������̼����Ԫ�ص�������11g��![]() ��8g�����ߵ�������Ϊ16g�����μӷ�Ӧ������������20g��8g��12g�����Կ��ж�W�к�����Ԫ�أ�����W������Ԫ����ɣ���C��ȷ
��8g�����ߵ�������Ϊ16g�����μӷ�Ӧ������������20g��8g��12g�����Կ��ж�W�к�����Ԫ�أ�����W������Ԫ����ɣ���C��ȷ
D��W��̼����Ԫ��ԭ�Ӹ�����Ϊ��![]() ��1��4����ȷ��
��1��4����ȷ��
��4������Ҫ98%Ũ��������Ϊx
28%��1000g��x��98%��1.84g/mL����ã�x��155.3mL



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��Ƽҵ������°������������Ƽ�����䲿�ֹ������£�
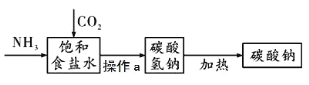
����Ҫ��Ӧԭ����
�� NaCl+H2O+NH3+CO2=NaHCO3��+NH4Cl
�� 2NaHCO3![]() Na2CO3+H2O+CO2�� �ȡ�
Na2CO3+H2O+CO2�� �ȡ�
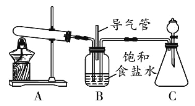
�������ϣ�ͨ������£�1L ˮ���ܽ�Լ 1L CO2 �� 700L NH3�� ij��ȤС���������ͼװ����ʵ����ģ����Ƽ���̣�����˵����ȷ����
���������Ƽ����ļ�ָ������������
�ڷ�Ӧԭ������Ӧ���������ܽ�ȵIJ���
����ͼ�У�B �е����ܵ�������ƽ����ѹ��C װ��������ȡ CO2
�ܸ��� NH3 �� CO2 �ܽ�ȵIJ�ͬ��Ϊ���ɸ���� NaHCO3��Ӧ����ͨ�� CO2 ��ͨ�� NH3
�ݲ��� a �������ǹ���
��Ӧԭ�����ʵ������� A װ���н���
��ҽ����NaHCO3 ����������θ�����
�෴Ӧ�����еĸ�����NH4Cl��ũҵ�ϳ��õĸ��Ϸ�
A.4 ��B.5 ��C.6 ��D.7 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ���Ϊ���г������ʣ���ת����ϵ����ͼ����������ʾ��һ������ת������һ�����ʣ���Ӧ���������ַ�Ӧ�������������ȥ����
![]()
��1�����ף��ҡ���������ͬһ�ֽ���Ԫ�أ�����ȱ������ƶѪ����Ϊ���ʣ��Һ�������Ԫ�أ�����������Ԫ�أ����������_____��
��2�����ס��ҡ�����Ϊ���и�Ԫ�صĻ��������ˮ��Ӧ�����Ҳ��ų��������ȡ����׳���_____��������ҵĻ�ѧ����ʽΪ_____����������_____��дһ�֣���
��3�����ס��ҡ���Ϊ���������Ԫ������һ��Ԫ�ؾ�����ͬ�����������ʳ���������Ϊ��̬����̬��Һ̬���������_____��дһ�֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ�������
A.�������͵������������������ƺ�������Һ����ֻ�Ϻ����Ȼ�����Һ��������ɫ����
B.�������ļ����һ����̼���ȼ�գ�һ����̼���ĵ���������
C.��������������������Ԫ�غ�����ȣ���������������Ԫ�ص�������Ϊ2��3
D.��һ�������ĸ�����ؼ���һ��ʱ����Թ�����Ԫ�غ���Ԫ�������ȿ���Ϊ11��12
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������þ�������ƵĻ����8g������һ����������������Һ��ǡ����ȫ��Ӧ����2.9g���������˺�������Һ�����ʵ���������Ϊ10%���Լ��㣺
��1��ԭ�����������þ����������________��
��2����������������Һ���ʵ���������_______��������������һλС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ƶ������dz��õ�ʵ���ֶ�
��1���������ϣ�С��������һ����ѧħ��������ɫֽ���������ɫС��A����ɫС��B����ɫС��C�Ϸֱ�������ɫ��M��Һ������ֽ���ֱ����˺�ɫ����ɫ����ɫ������ҺM�����ǣ�_____���ѧʽ����
��2��С���������ϵ�֪��ǣţ����������������ɫʯ��������Ƶ����ʡ���һ����ɫ��ǣţ�������ڷ���ˮ�ǣţ���ܿ����������һ��ǣţ�������ڼ�ͥ�������ij�ֳ��õ�ζƷ�У�ǣţ������˺�ɫ��������������ش�
�ٷ���ˮ��pH_____7����������������������������
��С��ѡ�õĵ�ζƷ������_____�������ƣ���
��3��һ����ɫ��ĩ�����������ơ�̼���ơ��Ȼ���������ͭ���������ơ��Ȼ����е�һ�ֻ�����ɡ�С��Ϊ�˲ⶨ�ð�ɫ��ĩ����ɣ����������ʵ�顣
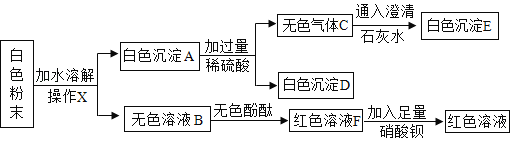
�������ͼʵ���������С���жϣ�
�ٲ���XΪ_____��
�ڰ�ɫ��ĩ�п��ܺ��е�������_____��
��д��C��E�Ļ�ѧ����ʽ_____��
�����ɫ��ҺF�м����������ᱵ��Ŀ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС���̽���ô���ʯ��ϡ���ᷴӦ��ȡ������̼���壬����������ʵ�顣ͼ1���й�ʵ��IJ���װ�ã������Ҫ��ش����⣺
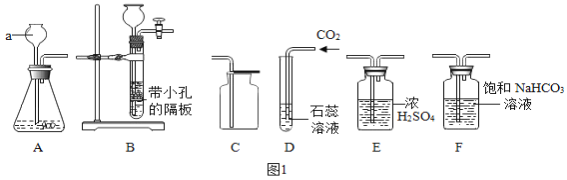
��1��a����������Ϊ______����ͬѧ��A��C�����ȡ������̼����ͬѧ��B��C�����ȡ������̼������Ϊ�Ǹ���ϸ����ڿ��Ʒ�Ӧ�ķ�����ֹͣ______����д���ң���
��2����ͬѧ����װ��D��������ʵ��ʱ���۲쵽��ɫʯ����Һ���ɫ������ɫҺ���ּ���δ�����±�Ϊ��ɫ������Ϊ���ܵ�ԭ����______��Ϊʹ������ɫҺ����Ⱥ������±�Ϊ��ɫ��������ͨ��װ��D֮ǰ�ɽ�����ͼװ��______������ĸ��ţ���
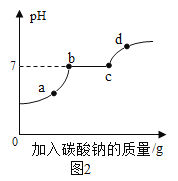
��3����ͬѧ����ȡ������̼��Ӧ�IJ�Һ�м���Na2CO3��Һ����ҺPH�仯��ͼ2��ʾ����ʾ���Ȼ�����Һ�����ԣ���a��ʱ����Һ�е����ʵĻ�ѧʽ��______������Na2CO3��Һ�Ĺ����й۲쵽������������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ճ����������Ź㷺����;�����������Ļ��˳����ͼ1��
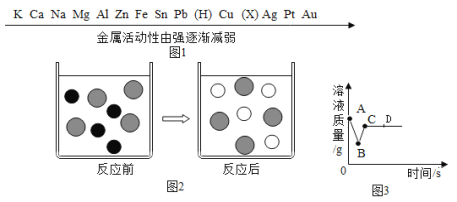
��ش��������⣺
��1���������˳���е�X��_____����Ԫ�ط��ţ���
��2������CuSO4��Һ�м��������FeƬ����ַ�Ӧ���ܹ۲쵽��������_____����ͼ2��ʾ�÷�Ӧǰ����Һ�д��ڵ���Ҫ���ӣ���д����ͼ�δ��������ӣ������ӷ��ţ���![]() ��_____������_____��
��_____������_____��
��3����һ������AgNO3��Cu��NO3��2�Ļ����Һ�м��������Zn�ۣ���Һ�����淴Ӧʱ��ı仯�����ͼ3��ʾ��ͼ��B����Һ�к��е�������_____���ѧʽ����ͬ����ͼ��D�������ɷ���_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����ϣ���Ҫ����50g 8%������������Һ�������ͼ�ش����⡣
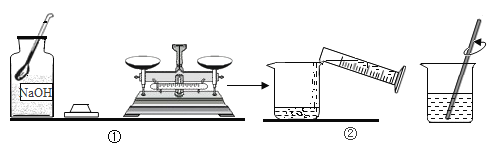
��1����ͼ��װ�ó����������ƹ��壬��ȷ�IJ�����_____������ţ���
Aֱ�ӷ��������ϳ���
B�ȳ���һ��С�ձ��������ٽ��������ƹ����������������
C�����������ϸ���һ�Ŵ�С��ͬ��ͬ��ֽ�����������ƹ����������ֽ�ϳ���
��2������ˮ�����Ϊ_____mL
��3������������������������_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com