

���� ��1����ͼ1��ʾ���۲쵽��������ƹ������Ƭ��ȼ�գ�ͨ����ʵ�飬˵��ȼ�յ�����֮һ�ǣ���ȼ��ﵽ�Ż���ȼ�գ�
��2������Ũ���ᡢŨ��ˮ���лӷ����Լ����ָʾ����������ɫ������н��
��3�������ܽ�ȵĸ��ÿ100��ˮ������ܽ����ʵ��������н��
��� �⣺��1����ͼ1��ʾ���۲쵽ͭƬ�ϵ�������ƹ������Ƭ��ȼ�գ�ͨ����ʵ�飬˵��ȼ�յ�����֮һ�ǣ���ȼ��ﵽ�Ż���ȼ�գ�
��2��ʵ��D���ձ����г��ֵ�������˵�������Dz����˶��ģ����ձ�����Һ��ʱŨ��ˮʱ��Ũ��ˮ���лӷ��ԣ��ӷ����İ�������ˮ�Լ��ԣ������ձ����еķ�̪��Һ����ɫ��Ϊ��ɫ�����ձ�����Һ�廻��Ũ���ᣬŨ������лӷ��ԣ��ӷ������Ȼ�����������ˮ�����ԣ��ձ�����Һ�廻�ɵ��з�̪NaOH��Һʱ��һ��ʱ�����Һ��ɫ�ı仯�Ǻ�ɫ����ȥ��Ϊ��ɫ������������NaOH��Ӧ�����Ȼ��ƺ�ˮ��Ҳ�������е�����������е�����������������ˮ��
��3��20��ʱ����ص��ܽ����63.9g����40��ʱ100gˮ������ܽ�����ص�������63.9g�����Ը��¶�������ر�����Һ�����ʵ���������=$\frac{63.9g}{100g+63.9g}$��100%=38.9%��
����ص��ܽ�����¶�Ӱ��ϴ����Կɲ�ȡ���½ᾧ�ķ�����þ��壮
�ʴ�Ϊ����1����ȼ��ﵽ�Ż���ȼ�գ����ȣ�
��2����ɫ����ȥ��Ϊ��ɫ��H++OH-�TH2O�����Աȣ�
��3��38.9%������
���� ������һ��ʵ������⣬����Ĺؼ�������ȼ�յ��������ᾧ�����������˶�������֪ʶ�Ĵ�Ǩ�ƣ�ֻ����������˳�����⣮


 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ��ij��Ӧ����ʾ��ͼ��������ʾ��ԭ�ӣ����ʾ��ԭ�ӣ��й�˵����ȷ���ǣ�������
��ͼ��ij��Ӧ����ʾ��ͼ��������ʾ��ԭ�ӣ����ʾ��ԭ�ӣ��й�˵����ȷ���ǣ�������| A�� | ͼ�мס��ҡ����������ʶ��������� | |
| B�� | ͼ�мס��ҡ����������ʾ����ɷ��ӹ��ɵ� | |
| C�� | �÷�Ӧǰ��������ࡢԭ�������û�иı� | |
| D�� | �÷�Ӧ��ѧ����ʽΪ2H202=2H20+02 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
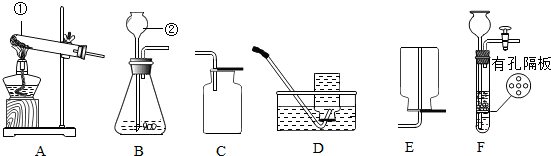
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��ˮ��Ӧ�����·� | B�� | ��ˮ������һ������ˮ | ||
| C�� | ��ˮ������Ϊ����ˮ | D�� | ��ˮ�ڵ�ˮ��ζ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ƹ� | B�� | ţ�� | C�� | ������ | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | �� | �� | �� |
| ��ҺA�е����� | NaOH | NaOH��Na2CO3 | NaOH��Ca��OH��2 |
| ��ɫ����B�ijɷ� | CaCO3 | CaCO3 | CaCO3 |
| ʵ�鲽�� | ʵ������ | ʵ����� |
| ȡ��ҺA���Թ��У����뼸��ϡHCl | �����ݲ��� | ���벻���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
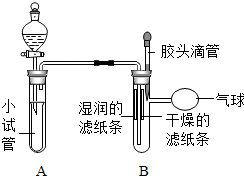 ��ͼ��ʾװ�õ�A�Թ��ڹ̶�һ��С�Թܣ����г���������ȥ��
��ͼ��ʾװ�õ�A�Թ��ڹ̶�һ��С�Թܣ����г���������ȥ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com