
| 影响因素 | 操作步骤 | 现象与结论 |
| 示例:浓度 | 在相同条件下,取两份相同质量的H2O2溶液,其中一份浓度为5%,另一份浓度为15% | 15%的H2O2 溶液分解速率明显比5%的H2O2 溶液的分解速率快,说明浓度能改变化学反应速率. |
| 影响因素 | 操作步骤 | 现象与结论 |
| 温度 | 取两份相同质量、相同溶质质量分数的H2O2溶液,对其中一份微热 | 被加热的H2O2 溶液分解速率明显比未加热的H2O2 溶液的分解速率快,说明温度能改变化学反应速率. |
| 催化剂 | 相同温度下,取两份相同质量、相同溶质质量分数的H2O2溶液,其中一份加入少量二氧化锰 | 放有二氧化锰的H2O2 溶液分解速率明显比未放二氧化锰的H2O2 溶液的分解速率快,说明催化剂能改变化学反应速率 |


科目:初中化学 来源: 题型:
 某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?乐山二模)某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:①称取25.0g石灰开佯品,平均分成两份,并分别加工成块状和粉末状; ②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如图所示:
(2012?乐山二模)某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:①称取25.0g石灰开佯品,平均分成两份,并分别加工成块状和粉末状; ②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:
| 影响速率的 因 素 | 例 证 | 影响速率的 因 素 | 例 证 | 影响速率的 因 素 | 例 证 |
| 物质本身的 性 质 | 温 度 | 浓 度 | |||
| 催 化 剂 | 接触面积 | / | / |
查看答案和解析>>
科目:初中化学 来源: 题型:
某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
①称取25.0g石灰开佯品,平均分成两份,并分别加工成块状和粉末状;
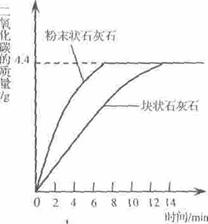
②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如下图所示:
请回答:
(1)每份样品充分反应后.生成二氧化碳的质量为 g;该样品中碳酸钙的质量分数为 %.
(2)若每份祥品中加入l00.0g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数。(要求写出计算过程.不考虑水、氯化氢的逸出.结果精确打0.1%)
解:
(3)由图中曲线分析得出,影响该化学反应速率的因索是:
请另外举出—个生活或生产中控制化学反应速率的实例:
查看答案和解析>>
科目:初中化学 来源: 题型:
某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:①称取25.0g石灰开佯品,平均分成两份,并分别加工成块状和粉末状; ②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如下图所示:
请回答:
(1)每份样品充分反应后.生成二氧化碳的质量为 g;该样品中碳酸钙的质量分数为 %.
(2)由图中曲线分析得出,影响该化学反应速率的因索是: ![]()
请另外举出—个生活或生产中控制化学反应速率的实例:
(3)若每份祥品中加入l00.0g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数。(要求写出计算过程.不考虑水、氯化氢的逸出.结果精确打0.1%)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com