
【题目】有关质量守恒定律的理解或应用正确的是
A. 10g 氢氧化钠溶液与 10g 硫酸铜溶液混合,得到 20g 溶液
B. 1g 碳酸钙粉末与 10g 水混合,形成 11g 溶液
C. 5g 硫和 5g 氧气在点燃条件下完全反应,生成物质量为 10g
D. 甲烷燃烧时,甲烷减少的质量等于生成的 CO2 和 H2O 的质量总和
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:初中化学 来源: 题型:
【题目】相同质量的M、N两种活泼金属,分别与足量质量分数为8%的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是
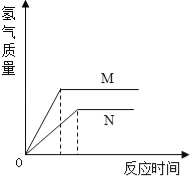
A. 金属的活泼性N>M
B. 两个反应生成H2的体积相等
C. 相对原子质量N>M
D. 两个反应消耗盐酸的质量一定相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】绿色植物的呼吸作用会产生二氧化碳,小明猜惑:种子的萌发过程可能也会产生二氧化碳,他设计了如图的实验装置.打开D装置中的阀门,水位下降,空气就会依次进入装置.
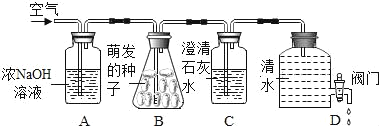
(1)A装置的作用是_____.
(2)如果观察到_____现象,则小明的猜想是正确的.
(3)请指出D装置的一个优点:_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学为测定石灰石样品中碳酸钙的质量分数,设计如下实验。用天平秤取12.5g石灰石样品放入小烧杯中;加入50g的稀盐酸,充分反应后称量剩余物的质量为58.1g,并测得溶液的pH值为4。
(1)测得溶液pH的目的是_____。
(2)求石灰石中碳酸钙的质量分数_____?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答有关问题。
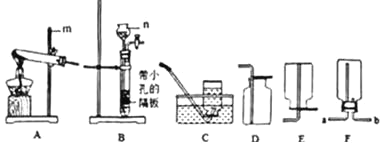
①写出编号仪器名称:m_____,n_____。
②实验室利用A装置可制取氧气,试管口略向下倾斜的原因是_____,反应的化学方程式为_____;若欲收集一瓶氧气,供铁在氧气中燃烧的实验使用,最好选用气体的收集装置中的_____(填装置编号),铁丝在氧气中燃烧的化学方程式为_____。
③实验室用B装置制备二氧化碳气体,反应的化学方程式为_____,用装置F收集二氧化碳,验满时,燃着的小木条应放在_____(填“a”或“b”)端;实验结束关闭B中活塞,B中的现象是_____。
④实验室制氢气常用锌与20%的稀硫酸反应,应选择的发生装置是_____(填编号),若要制取0.4克氢气,至少需要多少mol锌与足量的稀硫酸反应?_____(根据化学方程式计算)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某白色固体可能含有BaCl2(溶液显中性)、NaOH、Na2CO3、Na2SO4中的一种或几种,某小组同学为确定该白色固体的成分,进行如下探究。
①初步探究:实验设计如图所示。
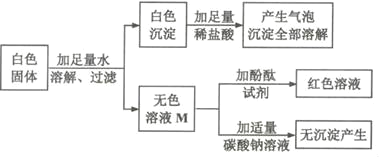
(初步结论)原白色固体中一定有的物质是_____。M溶液中的溶质一定有_____,一定没有氯化钡。
(交流讨论)甲同学认为:无色溶液M变红色,说明溶液M中含有碱性物质,但不能说明原白色固体中是否含有氢氧化钠,需要进一步确定。
②继续探究:无色溶液M中是否含有氢氧化钠?
(实验探究)
实验步骤 | 实验现象 | 实验目的 |
A.取溶液M于试管中,加入 _____,振荡,静置 | 白色沉淀 | _____ |
B.取实验A所得的上层清液于试管中,加入酚酞试剂。 | 清液变红色 | 证明溶液M中有氢氧化钠 |
通过实验,小组同学完成了本次探究活动。 | ||
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学反应的实质是构成物质分子的原子重新进行组合,形成新分子的过程。如图是在密团容器中某化学反应过程的微观示意图。据图回答:
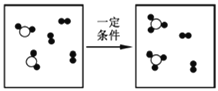
(1)参加反应的“![]() ”与“
”与“![]() ”的分子个数比为_________。
”的分子个数比为_________。
(2)该反应的基本反应类型是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有瓶过了保质期的淡黄色固体药品,标签上名称为“过氧化钠(Na2O2)”。某研究小组在老师指导下对其成分和性质进行如下探究。
(查阅资料)I.过氧化钠是一种淡黄色固体,常用在呼吸面具和潜艇中产生氧气。其原理是:2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2=2Na2CO3+O2
Ⅱ.常温、常压下O2的密度为1.3g/L。
(分析猜想)
(1)该小组同学认为,不做实验,就可以判断该物质中一定含Na2O2,理由是_____。
(2)进一步对固体成分提出以下猜想:I.只有Na2O2;Ⅱ.含有Na2O2、NaOH两种物质;Ⅲ.含有_____两种物质;Ⅳ.含有_____三种物质。
(实验探究)
按如图的所示连接好装置。用电子天平秤取2.00g样品于干燥的装置中,分液漏斗中添加一定量的蒸馏水。
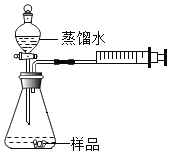
(3)打开分液漏斗活塞,将水滴加到锥形瓶中。反应完全后无固体剩余,注射器中收集到80mL气体,说明样品中含有_____gNa2O2(结果保留到小数点后两位,下同)。
(4)向反应后溶液中滴加酚酞,溶液显红色,说明反应后溶液显_____(选填“酸性”或“碱性”),小明认为原固样品体样品中一定含有氢氧化钠,你认为他的观点_____(选填“正确”或“不正确”),理由是_____。
(5)继续向锥形瓶中滴加足量的氯化钡溶液,有白色沉淀生成,静置,上层清液红色不褪,根据实验可以确定滴加酚酞溶液前锥形瓶中溶液含有的溶质是_____(填化学式)。
(6)将锥形瓶中混合物经过过滤、洗涤、干燥等,称得固体质量为1.97g。
(得出结论)
通过以上实验得出猜想_____成立。氢氧化钠的质量为_____g。
(反思与提高)
过氧化钠长期暴露在空气中,最终会变质为_____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】目前全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
Ⅰ.(镍粉制备)
工业用电解镍新液(主要含NiSO4,NiCl2等)制备碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O],并利用其制备镍粉的流程如下:
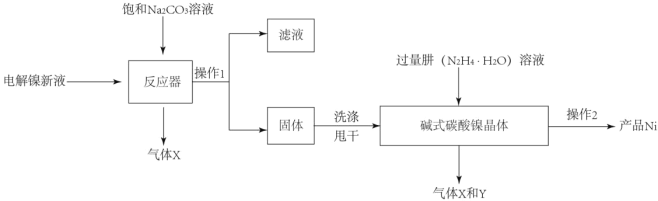
(1)反应器中的一个重要反应为3NiSO4+3Na2CO3+2H2O=NiCO32Ni(OH)2+3Na2SO4+2X,X的化学式为_____。
(2)物料在反应器中反应时需要控制反应条件。
分析下图,反应器中最适合的温度及pH分别为_____℃、_____。
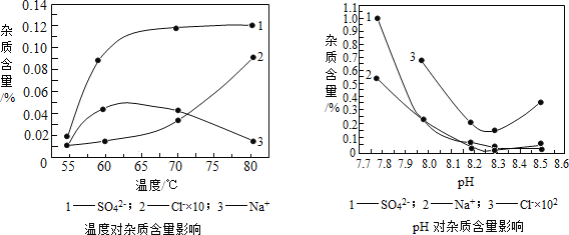
(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将_____(填“升高”、“降低”或“不变”)。
(4)操作2含过滤、水洗、95%酒精浸泡、晾干等操作,其中用95%酒精浸泡的目的是_____。
Ⅱ.(测定碱式碳酸镍晶体的组成)
为测定碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O]组成,某小组设计了如下实验方案及装置:
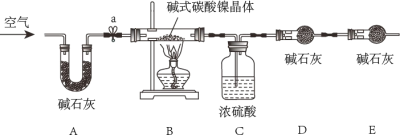
(资料卡片)
①碱式碳酸镍晶体受热会完全分解生成NiO、CO2和H2O
②碱石灰是NaOH和CaO的混合物,可以吸收CO2和H2O
(实验步骤)
①检查装置气密性;②准确称量3.77g碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O]放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;
④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)
装置C/g | 装置D/g | 装置E/g | |
加热前 | 250.00 | 190.00 | 190.00 |
加热后 | 251.08 | 190.44 | 190.00 |
(实验分析及数据处理)
(1)实验过程中步骤⑤鼓入空气的目的是_____。
(2)计算3.77g碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O]中镍元素的质量_____。最终通过计算得到了碱式碳酸镍晶体的组成。
(实验反思)
(3)另一小组同学加热时在酒精灯上加了铁丝网罩,实验结束后,称得装置B中残留固体质量明显增大。经查阅资料发现:在温度控制不当导致温度过高时,NiO会被氧化成Ni2O3。该组同学称得残留的固体中镍元素的质量分数可能是_____。
A 70.1% B 75.9% C 78.7% D 79.6%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com