
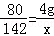 解得X=7.1g,
解得X=7.1g,

 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源:不详 题型:实验题
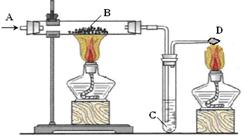
| 序号 | 探究实验 | 简答 |
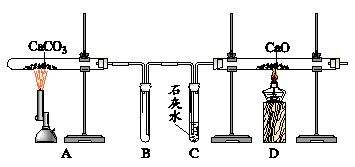
| Ⅰ | 若为H2与CuO的反应 | B处玻璃管观察到现象: 。 |
| Ⅱ | 若为CO与CuO的反应 | B处反应的化学方程式: , 发生氧化反应的物质是: 。 |
| Ⅲ | 若为CO2与C 的反应 (B处换成酒精喷灯加热) | B处的黑色粉末逐渐减少,最后消失, D处观察到有 色的火焰。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 金属 | 空气 | 稀硫酸 | 硝酸银溶液 |
| 铁 | - | √ | √ |
| 铜 | - | - | √ |
| 镁 | √ | √ | √ |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
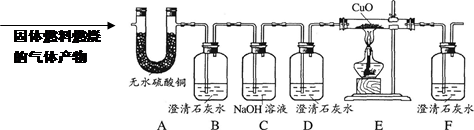
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 实验编号 | 硫酸的质量分数 (均取20mL) | 锌的形状 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
 2KCl+3O2↑。
2KCl+3O2↑。| 实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
| 1 | 0.6 | | 67 | 1800 |
| 2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
| 3 | 0.6 | g 氧化铁 | 67 | 89.5 |

| 装置 | 实验现象 | 实验分析 |
| A | 红色固体全部变黑 | 生成了铁 |
| B | 石灰水变浑浊 | 产生二氧化碳 |
| | 铁粉 | 氧化亚铁 | 氧化铁 | 四氧化三铁 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 磁性 | 有 | 无 | 无 | 有 |
| 与CO反应 | 不反应 | 反应 | 反应 | 反应 |
| 与稀盐酸反应 | 反应 | 生成氯化亚铁和水 | 生成氯化铁和水 | 生成氯化亚铁、氯化铁和水 |
| 与硫酸铜溶液反应 | 反应 | 不反应 | 不反应 | 不反应 |
| 步骤 | 实验操作 | 实验现象 | 结论和解释 |
| 1 | 用磁铁吸引剩余固体 | _____________ | 剩余固体中没有氧化亚铁。 |
| 2 | __________________ | ______________ | 剩余固体中只有铁粉。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.检验CO纯度时,没有听到响声,表明气体已纯净 |
| B.证明二氧化碳的密度比空气大,用烧杯罩住一支燃着的蜡烛 |
| C.鉴别双氧水和纯水,取样后分别加入MnO2,观察现象 |
| D.证明氧气是否集满,只能用带火星的木条的方法 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

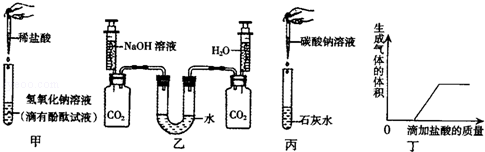
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com