

科目:初中化学 来源: 题型:选择题
| 结晶水合物 | 熔点/℃ | 熔化时吸热/(KJ•g-1) | |
| A | CaCl2•6H2O | 29.0 | 0.172 |
| B | Na2SO4•10H2O | 32.4 | 0.269 |
| C | Na2HPO4•12H2O | 36.1 | 0.282 |
| D | Na2S2O3•5H2O | 48.5 | 0.200 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
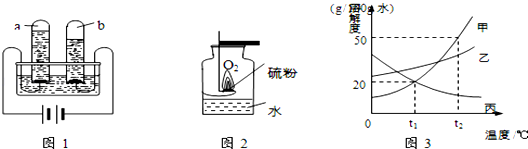
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在氧气中剧烈燃烧,生成四氧化三铁 | |
| B. | 少量高锰酸钾固体溶于水可得到蓝色溶液 | |
| C. | 硫在空气中燃烧发出蓝紫色火焰 | |
| D. | 向久置的氢氧化钠固体中滴加盐酸产生气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 (1)化肥尿素[CO(NH2)2]中碳、氧、氮、氢四种元素的原子个数比为1:1:2:4
(1)化肥尿素[CO(NH2)2]中碳、氧、氮、氢四种元素的原子个数比为1:1:2:4查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 肥料成份名称 | 用量(毫克∕升) |
| 硝酸钙 | 1260 |
| 硫酸钾 | 250 |
| 磷酸二氢钾 | 350 |
| 硫酸镁 | 537 |
| 硫酸铵 | 237 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com