t℃时,将一包质量为23.0克的Na2O和Na2CO3的混合物,加入到120克质量分数为18.25%的盐酸溶液中刚好完全反应,得到NaCl溶液.如果将该NaCl溶液蒸发掉31.5克水,刚好是t℃时的NaCl饱和溶液.
(1)写出氧化钠、碳酸钠分别与盐酸反应的化学方程式______、______.
(2)120克质量分数为18.25%的盐酸溶液中,氯化氢的质量是多少克?(精确到0.1克)
(3)求t℃时氯化钠的溶解度.(精确到0.1克)
解:(1)氧化钠和盐酸反应生成氯化钠和水,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,故答案为:Na
20+2HCl═2NaCl+H
20 Na
2C0
3+2HCl═2NaCl+H
20+CO
2↑;
(2)溶质质量等于溶液质量乘以质量分数,120×18.25%=21.9克,故答案为:氯化氢的质量21.9克;
(3)解:设氧化钠、碳酸钠分别与盐酸反应后生成氯化钠的质量为x,生成水的质量为y,t℃时氯化钠的溶解度为S
根据以上方程式可得以下二个关系式:
HCl~~~NaCl
36.5 58.5
21.9克 x
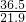
=
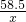
x=35.1克
2HCl~~H
20
73 18
21.9克 y
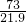
=
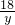
y=5.4克
120克盐酸溶液中水的质量120克-21.9克=98.1克
所以氯化钠饱和溶液中水的质量=98.1克+5.4克=103.5克
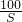
=
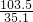
S=33.9克
答:氯化氢的质量为:21.9克,t℃时氯化钠的溶解度为33.9克.
分析:(1)根据题中的叙述找出反应物、生成物书写方程式;
(2)根据溶质质量等于溶液质量乘以质量分数进行分析;
(3)根据溶解度对应的是100克的溶剂进行分析.
点评:在解此类题时,首先分析题中考查的问题,然后根据题中的条件书写出方程式,再结合题中所给的数据列出比例关系求出相关的数据进行解答,注意溶解度对应的是100克的水.

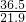 =
=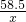
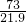 =
=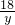
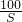 =
=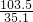


 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案