
| A、用氯化钡溶液区分稀盐酸和稀硫酸 |
| B、用灼烧法区分棉花和羊毛 |
| C、用熟石灰区分尿素和氯化铵 |
| D、用余烬木条区分二氧化碳和氮气 |


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案科目:初中化学 来源: 题型:
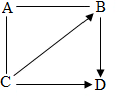 A、B、C、D为初中常见的物质,相互之间的关系如图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去)
A、B、C、D为初中常见的物质,相互之间的关系如图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去)查看答案和解析>>
科目:初中化学 来源: 题型:
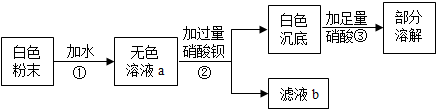
| A、由操作①可知:白色粉末中一定没有CaCO3、CuSO4 |
| B、由操作②可知:白色粉末中一定没有BaCl2 |
| C、由操作③可知:白色粉末中一定有K2SO4和K2CO3 |
| D、滤液b中的溶质有3种 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、用10mL量筒量取了5.26mL水 |
| B、用pH试纸测得某溶液的pH为8 |
| C、用托盘天平称取了16.35g氯化钠 |
| D、用温度计测得某溶液温度为22.45℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 选项 | 酸 | 碱 | 盐 | 氧化物 | |
| A | H2SO4 | Ba(OH)2 | H2S | H2O2 | |
| B | NaHCO3 | Cu2(OH)2CO3 | KCl | CO | |
| C | HNO3 | NaOH | CaCO3 | CuO | |
| D | HCl | Na2CO3 | CuSO4 | MnO2 | |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 4位同学的实验 | 甲 | 乙 | 丙 | 丁 |
| 加入氢氧化钠溶液质量 (g) | 29.0 | 34.5 | 40.0 | 45.0 |
| 反应得到沉淀的质量 (g) | 2.1 | 2.5 | 2.9 | 2.9 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
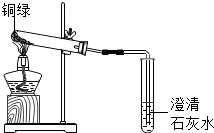 探究首饰中的金属
探究首饰中的金属| 实验步骤 | 可能观察到的现象 | 结 论 |
该“黄金”样品为黄铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com