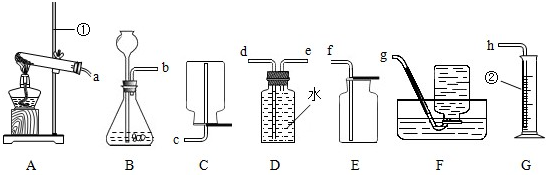
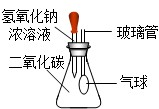
(2012?百色)化学小组同学对酸的性质很感兴趣,向老师提出研究硝酸的性质,老师高兴答应并带领同学们进行了硝酸性质的实验探究.
【实验设计】
(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变
红
红
色.
(2)将Zn片投入稀硝酸中,预计将产生H
2,其名称为
氢气
氢气
.
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO
3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B.
【提出问题】
(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?硝酸具有哪些特性?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成H
2.
(2)氮元素某些气态物质的物理性质
|
NH3 |
N2 |
NO |
NO2 |
| 顏色 |
无色 |
无色 |
无色 |
红棕色 |
| 溶解性 |
极易溶于水 |
不溶于水 |
不溶于水 |
可溶于水或硝酸 |
【猜想与分析】
(1)小明同学认为石蕊变色后又褪色的原因是由于试管不干净,含有其他杂质造成的,要证明小明的观点,应进行的操作是
取少量稀HNO3于干净的试管中,滴入石蕊试液.观察实验现象(或用干净的试管重复上述实验)
取少量稀HNO3于干净的试管中,滴入石蕊试液.观察实验现象(或用干净的试管重复上述实验)
.
(2)大家一致认同了红棕色气体B是NO
2,但对于无色气体A及变化的原因有不同的看法:
①小丽同学认为A是NH
3,但遭到大家的一致反对,原因是
NH3极易溶于水,大多数气体会溶解在稀HNO3中.且在常温下NH3不易被氧化成NO2
NH3极易溶于水,大多数气体会溶解在稀HNO3中.且在常温下NH3不易被氧化成NO2
;
②小强同学认为A是N
2,也遭到大家的一致反对,原因是
N2的化学性质比较稳定,常温下,N2在空气中不能氧化成NO2
N2的化学性质比较稳定,常温下,N2在空气中不能氧化成NO2
;
③经讨论,最终大家获得了A是NO的共识.NO遇氧变成NO
2的化学方程式为
2NO+O2=2NO2
2NO+O2=2NO2
.
【实验探究】小红同学对硝酸能与Cu反应很感兴趣,便取了一小块铜片投入稀HNO
3中,发现Cu溶解,也出现上述Zn与稀HNO
3反应的类似现象,确证生成了NO,并在老师的帮助下,测出恰好反应的Cu和HNO
3的质量比为8:21,由此获得了Cu与稀HNO
3的反应方程式为
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
.
【交流反思】根据探究结果,请你解释稀HCl跟铜不反应而稀HNO
3却能跟铜反应的原因
铜不与稀HCl发生置换反应,是因为铜的金属活动性弱于氢.而稀HNO3具有强的氧化性,能与Cu发生氧化还原反应,生成NO等.
铜不与稀HCl发生置换反应,是因为铜的金属活动性弱于氢.而稀HNO3具有强的氧化性,能与Cu发生氧化还原反应,生成NO等.
.



 (2012?淮北模拟)小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:
(2012?淮北模拟)小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究: