【答案】
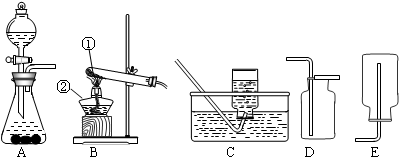
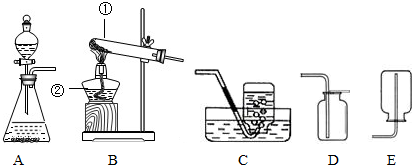
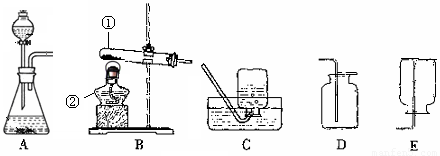
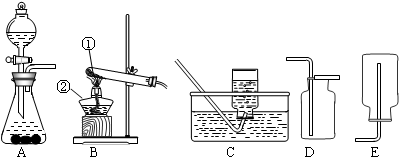
分析:(1)根据高锰酸钾需要在加热条件下反应的特点,选择制取氧气的发生装置;根据氧气密度大于空气且不易溶于水的性质,判断收集方法,选择收集装置;随着高锰酸钾的不断分解,颗粒越来越小,会随气体冲出试管,因此需要在管口放一团棉花进行过滤;
(2)根据装置图,辨识常见仪器并写出正确的仪器名称;
(3)根据装置A的使用特点固体与液体不需要加热,判断应用该装置制取氧气时所需要的药品;固体药品二氧化锰是反应的催化剂,放入锥形瓶里催化分液漏斗中滴入的过氧化氢分解会生成水和氧气;
(4)氯酸钾在加热条件下分解出氯化钾和氧气,由于反应速度较慢,可加入二氧化锰进行催化,加快反应的速度;制取时发生装置应选对固体加热型发生装置,收集时可选取向上排空气或排水法;制取的操作步骤为:连接装置-检验气密性-加入药品-加热-收集等操作;
(5)装置A的分液漏斗改为长颈漏斗时,为防止气体从长颈漏斗逸出,需要把漏斗伸入液面以下;在使用A装置制取气体时,应先把固体药品放入锥形瓶,再由分液漏斗滴入液体;而在组装B装置时,一般遵循由下到上、由左至右的原则进行组装;组装时根据仪器的使用要求,进行正确的连接以保护仪器;
(6)利用氧气能使带火星木条复燃的特性,把带火星木条放在瓶口可检验氧气是否收集满.
解答:解:(1)使用高锰酸钾制取氧气,需要进行加热,因此,发生装置应选B装置;随着不断分解,高锰酸钾颗粒逐渐变小而会随气体流出试管,此时,需要在管口放一团棉花进行过滤气体中的高锰酸钾;
故答案为:B;管口放一团棉花;防止高锰酸钾进入水槽;
氧气密度大于空气且不易溶于水,应采取C装置的排水法或D装置的向上排空气法进行收集;高锰酸钾在加热条件下,分解生成锰酸钾、二氧化锰和氧气;
故答案为:C或D;不易溶于水(或密度比空气大);高锰酸钾

锰酸钾+二氧化锰+氧气;KMnO
4
K
2MnO
4+MnO
2+O
2↑;
(2)仪器①用于对固体药品加热的试管;仪器②用于加热的仪器酒精灯;
故答案为:试管;酒精灯;
(3)装置A适用于固体与液体在常温下发生反应,选取A装置制取氧气应选用过氧化氢在二氧化锰催化下分解,液体过氧化氢从分液漏斗滴入,与放于锥形瓶内的二氧化锰接触而分解出水和氧气;二氧化锰在变化过程中起到加快反应速度的催化作用;
故答案为:过氧化氢;锥形瓶;二氧化锰;过氧化氢
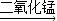
水+氧气;H
2O
2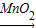
H
2O+O
2↑;催化作用;
(4)为加快氯酸钾的分解,可加入二氧化锰加快分解的速度,反应生成氯化钾和氧气;此时,应选取装置B作为反应的发生装置;由于氧气密度大于空气且不易溶于水,可采取C装置的排水法或D装置的向上排空气法进行收集;操作需要经过检查装置气密性,然后加入药品再进行加热和收集等操作;
故答案为:二氧化锰;氯酸钾
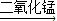
氯化钾+氧气;KClO
3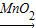
KCl+O
2↑;B;C或D;检查装置气密性;加入药品;加热;
(5)A、气体可以通过长颈漏斗逸出,因此,需要把长颈漏斗伸入到液面以下,进行液封;
故答案为:伸入液面以下;防止气体从长颈漏斗逸出;
B、在加入药品时,一般遵循先加固体药品后加液体药品的要求进行药品的加入;
故答案为:固体药品;液体药品;
C、组装装置时,应根据下面仪器的使用要求固定上面的仪器,根据左侧仪器的使用要求固体右侧的仪器,即由下至上、由左至右的组装方法;
使用试管对固体进行加热时,试管口要略向下倾斜,以防止水倒流而引起试管突然遇冷而炸裂;夹持试管的铁夹应夹在试管的中上部,以使试管受热均匀;加热时,应使用酒精灯火焰温度最高的外焰,先对试管进行预热然后对药品集中处加热;为收集到纯净的气体,在导管口的气体连续均匀放出时开始收集;收集完毕,为防止水槽内水倒吸入试管,应先把导管从水槽中撤出再停止加热;
故答案为:由下而上;从左到右;略向下倾斜;防止水倒流至管底使试管炸裂;试管的中上部;稍露出橡胶塞;外焰;预热;药品集中;气体均匀连续放出;撤出导管;停止加热;防止水倒流入试管引起试管炸裂;
(6)氧气能使带火星木条复燃,若放在瓶口的带火灾星的木条复燃,说明氧气已收集满;
故答案为:带火星的木条放在瓶口,木条复燃则收集满.
点评:本题对实验室制取气体的反应原理、仪器选用、装置连接等进行全方面考查,解答时要耐心细致.

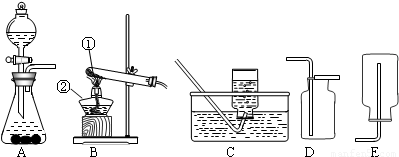
 锰酸钾+二氧化锰+氧气;KMnO4
锰酸钾+二氧化锰+氧气;KMnO4 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;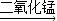 水+氧气;H2O2
水+氧气;H2O2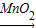 H2O+O2↑;催化作用;
H2O+O2↑;催化作用;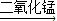 氯化钾+氧气;KClO3
氯化钾+氧气;KClO3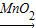 KCl+O2↑;B;C或D;检查装置气密性;加入药品;加热;
KCl+O2↑;B;C或D;检查装置气密性;加入药品;加热;