
 如图是同学们在实验室制作叶脉书签的部分操作步骤.请回答:
如图是同学们在实验室制作叶脉书签的部分操作步骤.请回答: 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:初中化学 来源: 题型:计算题
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入NaOH溶液的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
| 反应后溶液的质量/g | 144.5 | 164.5 | 179.6 | 189 8 | 200 | 220 |
| 每次产生沉淀的质量/g | 0 | 0 | m | n | 9.8 | 0 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
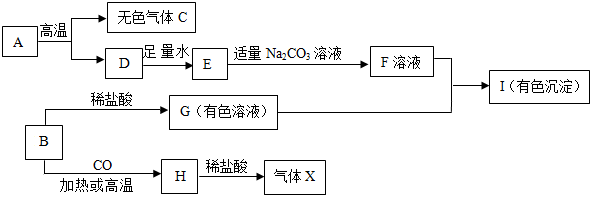
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分类观:纯碱和烧碱都属于碱 | |
| B. | 微粒观:氯化钠由钠离子和氯离子构成 | |
| C. | 元素观:一切物质都是由元素组成的 | |
| D. | 结构观:一氧化碳和二氧化碳分子不同,其化学性质不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 该反应类型为复分解反应 | |
| B. | 反应前后原子的种类和数目保持不变 | |
| C. | 该反应中反应物两种分子的个数比为3:1 | |
| D. | 图中表示化合物的是“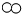 ” ” |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 实验操作 | 现象 | 结论 |
| A | 向久置空气中的NaOH固体滴加盐酸 | 产生气泡 | NaOH已部分变质 |
| B | 向某无色溶液滴入紫色石蕊试液 | 溶液变蓝 | 该溶液一定是碱溶液 |
| C | 将燃着的木条伸入盛满某气体的集气瓶中 | 木条熄灭 | 该气体是CO2 |
| D | 向碘化钾、稀硫酸和淀粉的混合液中加入某食用盐 | 溶液变蓝 | 该食用盐为加碘食盐 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com