
【题目】根据图的有关信息。请回答下列问题。
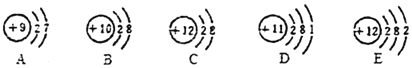
(1)微粒A、B、C、D、E共表示______种元素,属于同一种元素的是______(填编号下同);
(2)微粒A、B、C、D、E中,在化学反应中容易得电子的是______,表示阳离子的是______。
(3)A元素与E元素组成化合物的化学式是______。
(4)微粒E构成的单质在空气中燃烧时的现象是______。
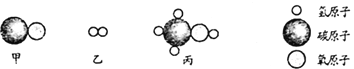
(5)甲和乙在催化剂、高温高压条件下反应生成丙,三种物质微观结构示意图如图2所示,该反应的化学方程式:______。
【答案】4 CE A C MgF2 发处耀眼的白光、生成了白色的固体,放出了大量的热 ![]()
【解析】
(1)由微粒的结构可知,微粒A、B、C、D、E中共有4种质子数,共表示4种元素,C、E的质子数相同,属于同一种元素;
(2)由微粒的结构可知,微粒A的最外层电子数是7,大于4,在化学反应中容易得电子,C的质子数=12>电子数=10,表示的阳离子。
(3)A元素是镁元素,化合价为+2价,E元素是氟元素,化合价为-1价,组成化合物的化学式是:MgF2。
(4)微粒E表示的元素是镁,构成的单质镁在空气中燃烧时的现象是:发处耀眼的白光、生成了白色的固体,放出了大量的热
(5)由微粒的结构可知,该反应是一氧化碳和氢气在催化剂、高温高压条件下反应生成甲醇,反应的化学方程式是:![]() 。
。


科目:初中化学 来源: 题型:
【题目】2018年11月28日,张家口一化工厂附近发生爆炸起火事故。消防人员使用水炮不断喷水,最终将大火扑灭。
(1)水炮灭火的主要原理是________。
(2)当地某化学兴趣小组想探究爆炸现场附近的空气中是否含有CO气体。
(查阅资料)二氧化碳不仅能与澄清的石灰水反应,而且还能与氢氧化钠溶液反应,因此,氢氧化钠溶液可用于吸收二氧化碳气体。
(实验原理)①除去收集的空气样品中的氧气;②利用CO与Fe2O3反应。
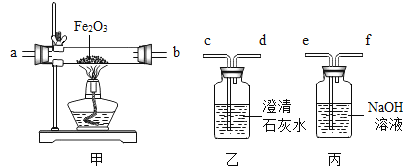
(表达与交流)①实验仪器的连接顺序是:丙→乙→甲→乙。其中乙装置使用两次,第一次的作用是___________。
②CO与Fe2O3反应的化学方程式为________。
③能判断出爆炸现场附近的空气样品中有较多CO的实验依据是__________或_________。
④从环境保护的角度考虑,你认为该实验的设计是否存在缺陷?如果有,该如何改进?_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】I.某化学兴趣小组进行如下系列实验。请根据下图回答问题:
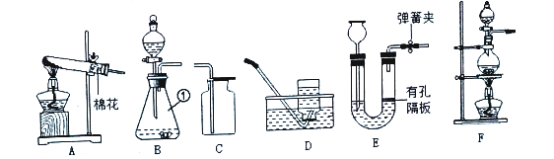
(1)图B中仪器①的名称是______,实验室用A装置制取氧气时,在试管口放一团棉花的目的是_____。
(2)实验室用双氧水制取氧气的化学反应方程式为________,若实验室制取CO2时能控制使反应随时发生或停止,应该选用的发生发生装置是_______(填序号)
(3)实验室常用生氯化铵溶液和亚硝酸钠(NaNO2)溶液混合加热制取氮气,应选用的制取装置是________.(填序号)。
II实验室有一瓶只含少量水的碳酸氢铵样品,为测定其中碳酸氢铵的质量分数,化学兴趣小组利用如下图所示装置进行实验(该装置气密性良好,装置B、C中所装药品均足量,碱石灰石氧化钙和氢氧化钠的混合物)。已知碳酸氢铵受热分解的化学方程式为:NH3HCO3![]() NH3↑+H2O↑+CO2↑,NH3能被酸溶液完全吸收。
NH3↑+H2O↑+CO2↑,NH3能被酸溶液完全吸收。
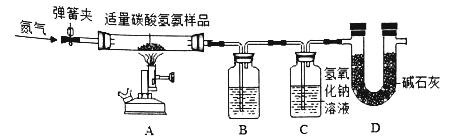
部分实验步骤如下
①打开弹簧夹,通入一段时间的氮气,测量B、C装置的质量;
②关闭弹簧夹,给碳酸氢铵样品加热;
③当样品反应完全,停止加热,再.....,直到玻璃管冷却,再次测量B、C装置的质量;
④实验完毕,测得装置B、C中药品的质量分别增加了3.6克、4.4克;
请回答下列问题:
(1)步骤①中通入氮气的目的是__,装置B中盛放的液体是_____,其作用是____。
(2)装置C中发生反应的化学方程式为____。
(3)步骤③中,停止加热后应进行的操作是___,如果缺少D装置,测得的碳酸氢铵的质量分数会_______(填“偏大”或“偏小”或“不变”或“无法确定”)。
(4)该样品中碳酸氢铵的质量分数为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Na+Cl2↑![]() 2NaCl表示钠在氯气中燃烧生成氯化钠的化学方程式,其中错误有:
2NaCl表示钠在氯气中燃烧生成氯化钠的化学方程式,其中错误有:
(1)____________________________;
(2)____________________________;
(3)____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A-F和X都是初中化学中的常见物质,其中A、C是元素组成相同的两种气体,B、F是红色固体,它们的转化关系如图所示(部分生成物已省略):

(1)请写出F的化学式_____________________;
(2)写出反应①的化学方程式___________________;
(3)写出②的化学方程式___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年10月24日上午,被称为“现代世界新七大奇迹”之一的港珠澳大桥正式通车运营。
(1)大桥建设过程中离不开吊装,吊装缆绳采用的超高分子聚乙烯纤维干法纺丝。聚乙烯的化学式为(C2H4)n,其中碳、氢元素的质量比为_____。
(2)大桥横跨“伶仃洋”。海洋中蕴含丰富的水资源,海水属于_____(填“纯净物”或“混合物”),我们可以通过_____操作除去海水中的难溶性杂质。检验海水是硬水还是软水的方法是_____。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年我省人大和政协两会使用了一种含碳酸钙的“石头纸”:为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。分别在5只烧杯中进行了实验,实验数据见下表(假设纸张其他成分既不溶于水,也不与酸反应):
烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
充分反应后生成气体的质量/g | 0.88 | 1.76 | 2.64 | 3.52 | 3.52 |
(1)10g样品与足量稀盐酸反应最多生成_____g气体;
(2)上述实验中盐酸过量的是烧杯_____(填序号);
(3)求样品中碳酸钙的质量分数_____。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碘化钾(KI)是白色固体,保存不当会被氧化为单质碘(I2)而泛黄变质。
化学小组查得以下资料:
I.对于碘化钾变质的原理,有两种不同的反应:
甲:4KI+O2+2CO2=2K2CO3+2I2 乙:4KI+O2+2H2O=4KOH+2I2
II.KOH与NaOH的化学性质相似。
II.K2CO3与稀疏酸的反应与实验室中制取二氧化碳反应原理类似。为探究碘化钾变质原理的合理性,开展以下实验。
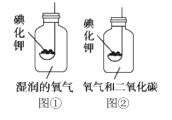
[实验过程]
[实验1]取适量碘化钾固体暴露于空气小一段时间,观察到固体泛黄。往泛黄的固体中加入足量稀硫酸,产生无色无味的气体,通入澄清石灰水中,澄清石灰水变浑浊。(1)化学小组认为:据此现象,还不能得出“反应甲是造成碘化钾变质的原因”的结论,因为有可能是反应乙生成的KOH继续与空气中的二氧化碳反应,写出该反应的化学方程式__________。
[实验2]按图①所示装置进行实验 ,数日后,观察到碘化钾固体无泛黄现象。
(2)据此现象,可得出的结论是__________
[实验3]按图②所示装置进行实验,数日后,观察到碘化钾固体无泛黄现象。
查阅文献获知,常温下某些气体和固体反应须在潮湿环境中进行。化学小组图①图②据此改进实验,很快观察到固体泛黄的现象。
(3)简述化学小组改进实验的具体措施:__________。
(4)根据上述实验,化学小组得出结论:碘化钾固体泛黄变质是碘化钾与______共同作用的结果。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是生产、生活中应用很广泛的一种金属。下列是与铁的性质有关的部分实验图,请回答下列问题。
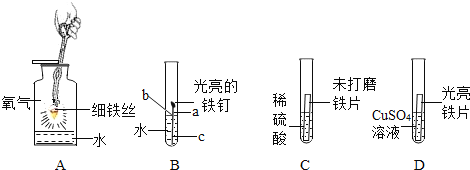
(1)A中集气瓶底部水的作用是______。
(2)①B中铁钉最易生锈的部位是______(填“a”“b”或“c”)。
②铝比铁活泼,但铝制品比铁制品更耐腐蚀,其理由是_______。
(3)C中刚开始无气泡产生,溶液颜色逐渐由无色变为黄色,此时试管内发生反应的化学方程式是______。
(4)写出D中反应的化学方程式______.
(5)探究实验:分别用不同量的锌加入到一定量的Mg(NO3)2、Cu(NO3)2、AgNO3混合溶液中,充分反应后过滤。以下是不同情况下对固体或和滤液成分的探究。①若向所得固体上滴盐酸有气泡产生,则该固体含有的金属为______。
②猜想:滤液中溶质为Mg(NO3)2、Zn(NO3)2、AgNO3,请分析该猜想不合理的原因是_____。
(6)将10g黄铜放入到100g稀盐酸的烧杯中,恰好完全反应后,测得烧杯中剩余物的质量为109.8g。计算稀盐酸的质量分数是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com