
 С��Ҫ�ⶨһƿϡ����������������������岽�����£�
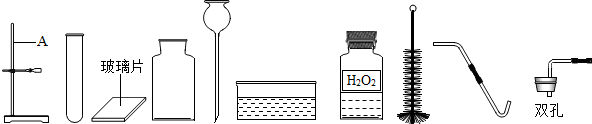
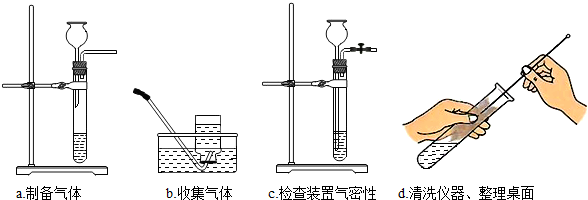
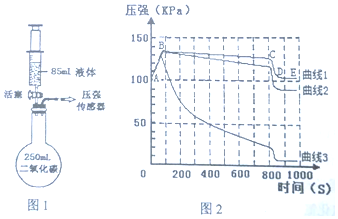
С��Ҫ�ⶨһƿϡ����������������������岽�����£����� ��1����Һ���ƹ����õ�������������ƽ���ձ�����Ͳ���������ͽ�ͷ�ιܣ�����Ҫ��ش���Dz�������
��2����A��ʱ��ʱ��Һ�����ԣ���������ʣ�࣬ͬʱ�������ɵ��Ȼ��ƣ�
��3����ͼ���Կ�������20g4%����������ʱǡ����ȫ��Ӧ�������������Ƶ������Ͷ�Ӧ�Ļ�ѧ����ʽ����HCl�����������������Ӧ������������
��4����������ƫ��Ҫôʱ���ʶ��ˣ�Ҫô���ܼ����ˣ�
��� �⣺
��1����Һ���ƹ����õ�������������ƽ���ձ�����Ͳ���������ͽ�ͷ�ιܣ���������
��2����A��ʱ��ʱ��Һ�����ԣ���������ʣ�࣬ͬʱ�������ɵ��Ȼ��ƣ�
��3����ͼ���Կ�������20g4%����������ʱǡ����ȫ��Ӧ�������������Ƶ�����Ϊ20g��4%=0.8g
��HCl������Ϊx
NaOH+HCl=NaCl+H2O
40 36.5
0.8g x
$\frac{40}{36.5}$=$\frac{0.8g}{x}$
x=0.73g
ϡ�����������������Ϊ$\frac{0.73g}{10g}$��100%=7.3%
��4��
�ٽ��������Ƶ����ձ�ʱ�������������������¹���ƫ�٣���������ƫС��
����ˮʱ���Ӱ�Һ�����������ƫ��ʵ�����ƫС������ˮ�����ˣ�������������ƫ��
�������ܽ���ձ��ڱ�δ��ָ����������ˮ�飬����ˮ���ˣ���������ƫС��
�ܳ���ʱʹ������������룬���¹���ƫ�٣���������ƫС��
��ѡ���ڣ�
�ʴ�Ϊ��
��1���ձ�����Ͳ���������ͽ�ͷ�ιܣ�
��2��HCl��NaCl��
��3��7.3%��
��4���ڣ�
���� ���ݻ�ѧ����ʽ����ʱ����һҪ��ȷ��д��ѧ����ʽ���ڶ�Ҫʹ����ȷ�����ݣ������������Ҫ������


 ������״Ԫ���Ծ�ϵ�д�
������״Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����¿���Fe��AgCl��Ӧ����ȡAg | |
| B�� | ���ù���Cu��OH��2��ȥCuSO4��Һ�л��е�����H2SO4 | |
| C�� | ���ܽ⡢���ˡ�����������IJ���˳����Գ�ȥ���������л��е��Ȼ��� | |
| D�� | ��ȥ������̼����������������һ����̼�����û�����建��ͨ������������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
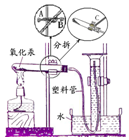 ��ͼ���о���ѧϰ���⡶��ѧ��Ӧ�������غ���о�����ʵ��װ�ã���ʵ��ͨ���ⶨ�������ֽ�ǰ��Ӧ���������������Ƿ��������֤�����غ㶨�ɣ���֪���������ֽ�ķ�Ӧ����ʽ��2HgO$\frac{\underline{\;\;��\;\;}}{\;}$2Hg+O2���������йر�ʵ�������������ǣ�������
��ͼ���о���ѧϰ���⡶��ѧ��Ӧ�������غ���о�����ʵ��װ�ã���ʵ��ͨ���ⶨ�������ֽ�ǰ��Ӧ���������������Ƿ��������֤�����غ㶨�ɣ���֪���������ֽ�ķ�Ӧ����ʽ��2HgO$\frac{\underline{\;\;��\;\;}}{\;}$2Hg+O2���������йر�ʵ�������������ǣ�������| A�� | ����Ͳ�м���һЩú�ͣ����Լ���������ˮ�е��ܽ� | |
| B�� | ���Ϲܿڷų��������ȵ����ݺ�����ռ����� | |
| C�� | ������δ�ֽ���ȫ��ֹͣ���ȶ�ʵ����û��Ӱ�� | |
| D�� | ���Ϲ�������Ͳ�ײ�����ʹ�ⶨ���������ȷ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ѧ��ȤС���ͬѧȡһ������ij��ʽ̼��ͭ���塾Cu2��OH��2CO3•2H2O��Ͷһ������ˮ�У�����������μ���ϡ���ᣮ����������õ������ԭ������H��1C��12O��16Na��23Cl��35.5Cu��64��
��ѧ��ȤС���ͬѧȡһ������ij��ʽ̼��ͭ���塾Cu2��OH��2CO3•2H2O��Ͷһ������ˮ�У�����������μ���ϡ���ᣮ����������õ������ԭ������H��1C��12O��16Na��23Cl��35.5Cu��64���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
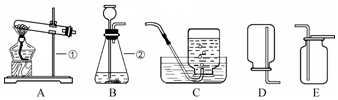
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 | |
| �ܽ��/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 59.5% | B�� | 10% | C�� | 25% | D�� | 16% |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com