
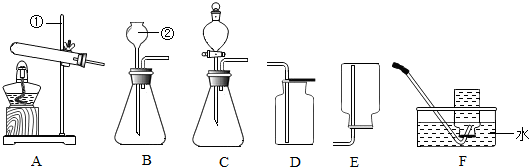
分析 (1)据常用仪器回答;
(2)用过氧化氢溶液制取氧气属于固液常温型,分液漏斗可控制滴加液体的速度,从而控制反应速率,据反应原理书写方程式;
(3)加热氯酸钾制取氧气属于固体加热型,故选发生装置A,氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集,据反应原理书写方程式;
(4)用碳酸钙和稀盐酸制取二氧化碳属于固液常温型,故选发生装置B,二氧化碳密度比空气大且能溶于水,所以可用向上排空气法收集,据反应原理书写方程式.
解答 解:(1)标号仪器分别是铁架台和长颈漏斗;
(2)用过氧化氢溶液制取氧气属于固液常温型,分液漏斗可控制滴加液体的速度,从而控制反应速率,故选发生装置C,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)加热氯酸钾制取氧气属于固体加热型,故选发生装置A,氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集;氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,反应方程式是:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)用碳酸钙和稀盐酸制取二氧化碳属于固液常温型,故选发生装置B,二氧化碳密度比空气大且能溶于水,所以可用向上排空气法收集,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应方程式是:CaCO3+2HCl=CaCl2+CO2↑+H2O;
故答案为:(1)铁架台;长颈漏斗;
(2)C;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)AD(或AF)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)BD(或CD);CaCO3+2HCl=CaCl2+CO2↑+H2O.
点评 本题着重考查了装置选取和反应原理,发生装置据反应物状态和反应条件进行选择,收集装置据气体的密度和溶解性选择.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
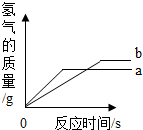 等质量的 a、b两种金属分别和足量的同体积、同浓度的稀盐酸反应,产生氢气的质量与时间的关系如图所示(a、b在生成物中化合价均为+2价).下列说法中不正确的是( )
等质量的 a、b两种金属分别和足量的同体积、同浓度的稀盐酸反应,产生氢气的质量与时间的关系如图所示(a、b在生成物中化合价均为+2价).下列说法中不正确的是( )| A. | 金属活动性:a>b | B. | 最终产生氢气的质量:a<b | ||
| C. | 相对原子质量:a>b | D. | 最终消耗稀盐酸的质量:a=b |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
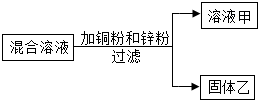 向一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则下述四种说法正确的个数为( )
向一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则下述四种说法正确的个数为( )| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
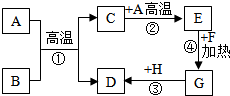 A-H是初中化学常见的物质,已知A是黑色固体单质,G为紫红色固体单质,B为红褐色粉末,F为黑色粉末,它们的转化关系如图所示.请回答:
A-H是初中化学常见的物质,已知A是黑色固体单质,G为紫红色固体单质,B为红褐色粉末,F为黑色粉末,它们的转化关系如图所示.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com