
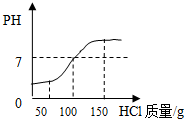
 把一定质量的混有NaOH和NaCl的固体放入烧杯中,加入足量水配成一份100g溶液,滴入酚酞使溶液变红,再逐渐加入3.65%的HCl溶液,所加入的HCl质量与溶液的PH变化如右图所示.当溶液刚好褪成无色时,测得溶液的溶质质量分数是10.925%.
把一定质量的混有NaOH和NaCl的固体放入烧杯中,加入足量水配成一份100g溶液,滴入酚酞使溶液变红,再逐渐加入3.65%的HCl溶液,所加入的HCl质量与溶液的PH变化如右图所示.当溶液刚好褪成无色时,测得溶液的溶质质量分数是10.925%.

 ×100%=20%
×100%=20%

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源: 题型:阅读理解
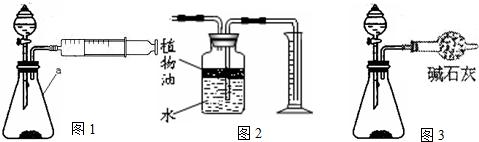
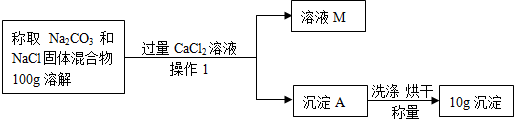
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com