
| A. | ①② | B. | ②③ | C. | ①②④ | D. | ①②③④ |
分析 根据影响化学反应速率的因素很多,使用相同的催化剂,就可以探究温度对H2O2分解速率的影响.在探究FeCl3与CuCl2+对H2O2分解的催化效果是,必须保持其他的条件相同解答.
解答 解:影响化学反应速率的因素很多,用相同的催化剂,但温度不同,所以反应速率不同是由温度不同导致的,所以可以探究温度对H2O2分解速率的影响,同样在探究FeCl3与CuCl2对H2O2分解的催化效果时,必须保持其他的条件相同,如:①实验温度;②H2O2的浓度;③催化剂质量;④FeCl3与CuCl2的颗粒大小.
答案:D.
点评 本题通过保持其他外界条件一致而改变一个条件来探究温度、催化剂对反应速率的影响,综合性较强,难度适中.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:初中化学 来源: 题型:多选题
| A. | 该无色气体可能为CH4 | B. | 该无色气体可能为H2、CO | ||
| C. | 该无色气体可能为CO和CH4 | D. | 该无色气体可能为H2、CH4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu2+、NH4+、Cl-、NO3- | B. | H+、K+、CO32-、SO42- | ||
| C. | H+、Na+、OH-、SO42- | D. | Na+、Ca2+、NO3-、CO32- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
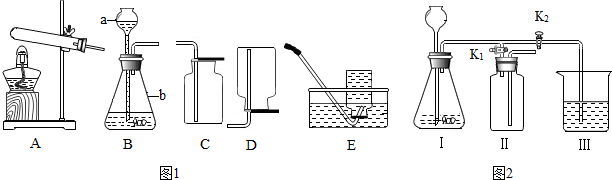
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 事 实 | 解 释 |
| A | 八月十五桂花香 | 分子不停地运动 |
| B | 物质的热胀冷缩现象 | 分子间的间隔改变 |
| C | 1个水分子的质量约是3×10-26kg | 分子的质量很小 |
| D | 25m3的氧气可以装入0.024m3的钢瓶中 | 氧分子的体积变小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com