
| A. | 属于氧化物 | |
| B. | 由两个金属元素和一个非金属元素组成 | |
| C. | 铁元素化合价为+6 | |
| D. | 其中钠、铁、氧元素质量比是2:1:4 |
分析 A.氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
B.根据元素的规定来分析.
C.根据化合物中元素化合价的计算方法来分析解答.
D.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
解答 解:A.高铁酸钠是由钠、铁、氧三种元素组成的化合物,属于氧化物,故选项说法错误.
B.元素是个宏观概念,只讲种类、不讲个数,故选项说法错误.
C.化合物中个元素化合价代数和为零,则有(+1)×2+铁的化合价+(-2)×4=0,即铁的化合价是+6价,故选项说法正确.
D.钠、铁、氧三种元素质量比是(23×2):56:(16×4)≠2:1:4,故选项说法错误.
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:初中化学 来源: 题型:解答题
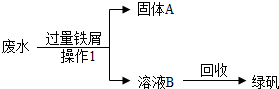 某工厂排出的废水中含有硫酸、硫酸铜,小艳同学取水样后进行研究性学习,请回答下列问题:
某工厂排出的废水中含有硫酸、硫酸铜,小艳同学取水样后进行研究性学习,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 发霉的大米蒸煮后食用 | |
| B. | 我们不要喝含汞、铅超标的水 | |
| C. | 用福尔马林保存海鲜 | |
| D. | 对于人体必需的元素摄入量越多越好 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
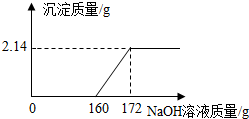 工业盐酸中通常溶有少量的FeCl3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl3与NaOH反应的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl.请回答下列问题:
工业盐酸中通常溶有少量的FeCl3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl3与NaOH反应的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
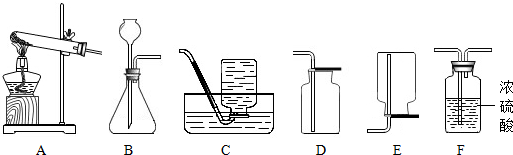
| 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀硫酸质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体质量/g | 26.75 | 23.5 | 20.25 | 17 | 16.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com