
| |||||||||||||||||||||||||
(1) |
答案:误认为物质都是由原子直接构成的,原子是一个实心球体,不可再分割 没有发现带正电荷的原子核 讲析:根据同学们学过的知识:“原子是由居于原子中心带正电荷的原子核和核外带负电荷的电子构成的”,可以推知道尔顿的原子论存在的缺陷是:①物质都是由原子直接构成的;②原子是一个实心球体,不可再分割.汤姆生只发现了原子内部的电子,但是他没发现带正电荷的原子核. |
(2) |
如果原子核是实心的球体,那么大多数α粒子不可能穿透金箔,而科学实验的结果却是大多数α粒子能穿透金箔而不改变原来的运动方向,说明原子核一定不是实心的球体. |
(3) |
答案:科学是不断向前发展的;科学发展的过程并不是一帆风顺的,而是要经过曲折而漫长的过程;任何一种科学理论都不是完美的,都或多或少有一定的缺陷;对待前人的知识或理论我们要用科学的态度来认识(答案合理即可) 讲析:此问只要答案合理,没有科学性错误均可. 点评:本题以科学发展史为命题背景,进行创新设问.解题时关键是灵活运用所学知识并深挖题给信息,从不同角度思考问题,并学会用辩证思维分析科学发展的曲折性,通过解题升华学生的情感,培养学生的科学精神和科学态度. |


科目:初中化学 来源:中考必读·名校备考方案·化学 题型:059
| |||||||||||||||||||||||||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
人类对原子结构的认识是逐渐深入的。下图所示是不同时期科学家提出的原子结构模型。

1808年,英国科学家道尔顿提出了原子论。他认为物质都是由原子直接构成的;原子是一个实心球体,不可再分割;同一类原子性质相同;不同的原子是以简单的整数比相结合。
1897年,英国科学家汤姆生发现原子中存在电子。1904年汤姆生提出了一个被称为“西瓜式”结构的原子结构模型,电子就像“西瓜子”一样镶嵌在带正电的“西瓜瓤”中。电子的发现使人们认识到原子是由更小的粒子构成的。
1911年英国科学家卢瑟福做了一个实验:用一束质量比电子大很多的带正电的高速运动的α粒子轰击金箔,结果是大多数α粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,还有极少数的α粒子被反弹了回来。据此他提出了带核的原子结构模型:原子是由原子核和核外电子构成。
……
根据以上材料,请回答:
(1)道尔顿提出了原子论,汤姆生发现了原子中的电子,这在当时是件很了不起的事,但由于受到那时科学技术水平的限制,他们的理论中存在一些缺陷甚至错误,按照目前初中阶段你学的原子结构的理论,你认为道尔顿的原子论存在的缺陷是
;汤姆生原子结构模型的缺陷是
。
(2)根据卢瑟福的实验所产生的现象,不能够获得的结论是 。
A.原子核体积很小 B.原子核质量较大
C.原子核带有正电 D.核外电子带有负电
(3)通过人类认识原子结构的历史,你对科学的发展有哪些感想?
。
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
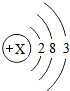 ,该元素与空气中含量居第二多的元素组成的化合物的化学式为________.
,该元素与空气中含量居第二多的元素组成的化合物的化学式为________.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

 D.原子结构示意图为
D.原子结构示意图为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com