
 如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:
如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:分析 (1)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)据该温度下A的溶解度分析解答;
(3)不饱和溶液变为饱和溶液可采取加入水或降温的方法;
(4)据A的溶解度随温度降低而减小,硝酸铵溶于水使溶液的温度降低解答;
(5)A的溶解度随温度升高而增大,所以要使其从饱和溶液中析出可采取降温的方法;
(6)t2℃时AB的溶解度相等,所以用50gA、B分别制成饱和溶液,需要水的质量相等;
(7)据该温度下B的溶解度和溶质的质量分数计算方法分析解答;
(8)等质量的饱和溶液降低相同的温度,溶解度变化大的析出晶体多,溶解度随温度降低而增大的无晶体析出,并据溶液中溶质的质量分数解答;
(9)据溶液稀释前后溶质的质量相等及溶质的质量分数计算方法分析解答;
(10)据物质的溶解度随温度变化可分析提纯物质的方法;
(11)氯化钾是由氯离子和钾离子构成 的化合物,并结合离子的写法解答;
(12)气态物质的溶解度随温度升高而减小,据此分析解答;
(13)将t1℃时A、B、C三种物质的饱和溶液升温至t2℃(溶剂量不变),AB的溶解度增大,溶液中溶质的质量不变,溶质的质量分数不变.
解答 解:(1)t2℃时,A、B、C三种物质的溶解度大小关系是A=B>C.
(2)t3℃时A的溶解度是80g,即100g水中最多溶解40g的A,所以将30gA物质加入到50g水中,充分溶解后,所得溶液是不饱和溶液.
(3)室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水中加入一定量的NH4NO3并搅拌,硝酸铵溶于水使溶液的温度降低,A的溶解度减小,所以试管内有固体A析出.
(4)A的溶解度随温度升高而增大,所以要使A的饱和溶液变为不饱和溶液,除加水之外还可采用升高温度的方法.
(5)A的溶解度随温度升高而增大,所以要使其从饱和溶液中析出可采取降温的方法.
(6)t2℃时AB的溶解度相等,所以用50gA、B分别制成饱和溶液,需要水的质量相等;
(7)t2℃时B的溶解度是60g,所以将100g水加入盛有50gB物质的烧杯中,充分溶解后,得到B的不饱和溶液.保持温度不变,往该烧杯中再加入10g水,充分搅拌后,B溶液中溶质的质量不变,溶剂的质量增加,所以溶质的质量分数 变小.
(8)t3℃时,将等质量A、B、C三种物质的饱和溶液降低到t1℃,C的溶解度变大,则没有晶体析出,溶液中溶质、溶剂的质量不变,则溶质质量分数不变,A的溶解度变化比B大,析出晶体最多.
(9)t2℃时A的溶解度是60g,即160g饱和溶液中溶质的质量是60g,设140g饱和溶液中A的质量是x,则有$\frac{160g}{60g}$=$\frac{140g}{x}$,解得x=52.5g;
溶液加水稀释过程中溶质的质量不变,设把t2℃时140gA的饱和溶液稀释为20%,需加水 的质量为y,则有52.5g=(140g+y)×20%,解得y=122.5g;
(10)A的溶解度受温度影响较大,B的溶解度受温度影响不大,所以A中含有少量的B,若要提纯A,可采用降温结晶的方法.
(11)若A是KCl,氯化钾是由氯离子和钾离子构成 的化合物,钾离子带一个的正电荷,氯离子带一个单位的负电荷,则A溶液中的溶质粒子是K+、Cl-;
(12)C的溶解度随温度升高而减小,可能是气态物质.
(13)将t1℃时A、B、C三种物质的饱和溶液升温至t2℃(溶剂量不变),AB的溶解度增大,溶液中溶质的质量不变,溶质的质量分数不变.
故答案为:
(1)A=B>C;(2)不饱和;(3)有固体A析出;(4)升高温度;(5)降温;(6)=;(7)不饱和;减小;
(8)C;AB;A;(9)122.5;(10)降温;(11)K+、Cl-;(12)C;(13)
点评 本题较为综合的考查了溶解度概念、离子的书写、物质的提纯、溶解度曲线知识的应用等知识,能很好的考查学生对知识的掌握和运用能力,是一道不错的综合题,解答时要结合所学知识细心分析解答.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:初中化学 来源: 题型:选择题
| A. | 碳原子核,含7个质子,8个中子 | B. | 氮原子核,含7个质子,7个中子 | ||
| C. | 碳原子核,含6个质子,7个中子 | D. | 氧原子核,含7个质子,8个中子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
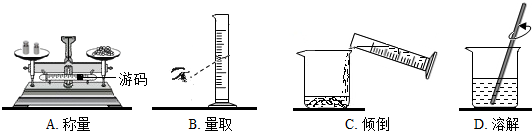
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 回答下列问题:
回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
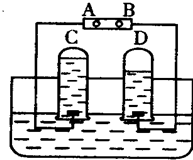 如图是电解水的简易装置.回答下列各问题:
如图是电解水的简易装置.回答下列各问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化作用 | B. | 作反应物 | C. | 作催化剂 | D. | 提供热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com