
分析 (1)根据水果和蔬菜所含的营养元素进行解答;
(2)根据活性炭具有吸附性进行分析;
(3)根据分子是运动的性质分析;
(4)根据酒精燃烧生成二氧化碳和水进行分析解答.
解答 解:(1)青少年要多吃蔬菜、水果,因为其中富含的营养素是维生素.
(2)净化水时使用活性炭,这是利用了活性炭的吸附作用.
(3)由于分子是运动的,温度越高,分子运动的越快,所以,蔗糖在热水中溶解快.
(4)酒精燃烧生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
故答案为:(1)维生素;(2)吸附;(3)温度越高,分子运动的越快;(4)C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
点评 化学与我们的生活息息相关,与生产、生活相关的知识是中考考查的热点之一,灵活运用所学知识是正确解答本题的关键.


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:初中化学 来源: 题型:选择题
| A、对鉴别方法的认识 | B、对安全的认识 |
| ①区分硬水和软水,加肥皂水后搅拌 ②区分棉纤维和羊毛纤维,点燃后闻气味 ③区分硫酸铵和硫酸钾,加熟石灰粉末研磨 | ①点燃可燃性气体前一定要验纯 ②煤矿矿井要保持通风、严禁烟火 ③生产面粉、铁粉的工厂不必禁火 |
| C、对现象的认识 | D、对防锈的认识 |
| ①气体压缩,是因为气体分子之间的间隔变小 ②柠檬汁使紫色石蕊试液变红,是因为柠檬汁呈酸性 ③喝汽水打嗝,是因为气体溶解度随温度升高而增大 | ①自行车的支架喷油漆防锈 ②保留铁锈可防止铁进一步锈蚀 ③菜刀用后及时洗净擦干 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
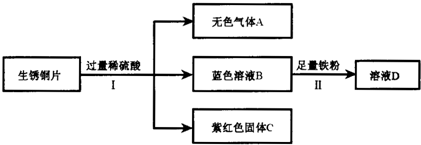
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
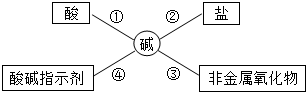 为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请完成下列问题.
为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请完成下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
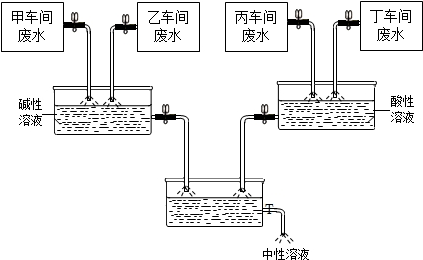
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 氢氧化钠溶液的质量/g | 4 | 12 | 16 | 28 | 32 |
| 生成沉淀的质量/g | 0 | 0.145 | 0.29 | 0.58 | 0.58 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com