
 表示氯原子
表示氯原子 表示钠原子
表示钠原子 表示氧原子
表示氧原子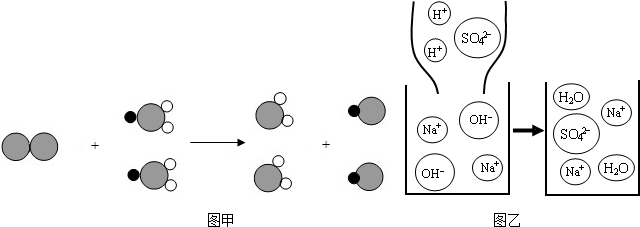


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:初中化学 来源: 题型:
 表示氯原子
表示氯原子 表示钠原子
表示钠原子 表示氧原子
表示氧原子
查看答案和解析>>
科目:初中化学 来源: 题型:
| 物质 | 氧气 | 水 | 铁 | 金 |
| 熔点/℃ | -218 | 0 | 1535 | 1064 |
| 沸点/℃ | -183 | 100 | 3000 | 2707 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 化学是研究物质组成、结构、性质及其变化规律的科学.请回答下列问题:
化学是研究物质组成、结构、性质及其变化规律的科学.请回答下列问题:
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com