
| 温度/℃ | 20 | 40 | 60 | 80 |
| 溶解度/g | 1.68 | 3.73 | 7.3 | 13.4 |
| A. | 高氯酸钾属于易溶于水的物质 | |
| B. | 高氯酸钾的溶解度随温度的升高而增大 | |
| C. | 40℃时,将2g高氯酸钾溶于98g水中所得溶液浓度为2% | |
| D. | 80℃时,113.4g高氯酸钾饱和溶液冷却至60℃,能析出6.1g晶体 |
分析 A、根据20℃时高氯酸钾的溶解度为1.68g进行解答;
B、根据图表可知高氯酸钾的溶解度随温度升高而增大进行解答;
C、根据40℃时,高氯酸钾的溶解度为3.73g,进行解答;
D、根据图表可知高氯酸钾的溶解度随温度降低而减小进行解答.
解答 解:A、20℃时高氯酸钾的溶解度为1.68g,所以高氯酸钾属于可溶于水的物质,故错误;
B、根据图表可知高氯酸钾的溶解度随温度升高而增大,故正确;
C、40℃时,高氯酸钾的溶解度为3.73g,所以40℃时,将2g高氯酸钾溶液于98g水,高氯酸钾完全溶解,溶液的浓度为$\frac{2g}{98g+2g}×100%$=2%,故正确;
D、根据图表可知高氯酸钾的溶解度随温度降低而减小,80℃时,高氯酸钾的溶解度为13.4g,60℃时,高氯酸钾的溶解度为7.3g,所以80℃113.4g高氯酸钾饱和溶液中含水100g、高氯酸钾13.4g,冷却至40℃有13.4g-7.3g=6.1g结晶现象,故正确.
故选:A.
点评 解答本题关键是要知道溶解度的含义,知道饱和溶液的容质质量分数计算方法,只要饱和溶液降温后溶解度减小了,就会析出晶体.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题

| A. | X的值为22 | B. | W由碳、氢、氧三种元素组成 | ||
| C. | W由碳、氢两种元素组成 | D. | 该反应属于置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 S2-;
S2-;查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是测定空气中氧气体积分数的实验装置示意图,已知集气瓶的容积约为320mL,实验结束时流入集气瓶中水的体积约为60mL.下列有关说法错误的是( )
如图是测定空气中氧气体积分数的实验装置示意图,已知集气瓶的容积约为320mL,实验结束时流入集气瓶中水的体积约为60mL.下列有关说法错误的是( )| A. | 红磷燃烧时产生浓厚的白烟,放出大量的热 | |
| B. | 燃烧结束,等集气瓶冷却到室温后松开弹簧夹读数 | |
| C. | 流入集气瓶中水的体积约等于磷燃烧消耗氧气的体积 | |
| D. | 本实验中,测出空气中氧气的体积分数约为21% |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 某校学习小组为测定某石灰石样品中CaCO3的质量分数,取12.5克石灰石样品与足量稀盐酸反应.反应过程中生成二氧化碳气体的质量随反应时间的变化如图所示.请你利用图示信息,回答下列问题和计算:
某校学习小组为测定某石灰石样品中CaCO3的质量分数,取12.5克石灰石样品与足量稀盐酸反应.反应过程中生成二氧化碳气体的质量随反应时间的变化如图所示.请你利用图示信息,回答下列问题和计算:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 现在空气的成分 | N2、O2、CO2水蒸气及惰性气体等 |
| 原始大气的主要成分 | CH4、NH3、CO、CO2等 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
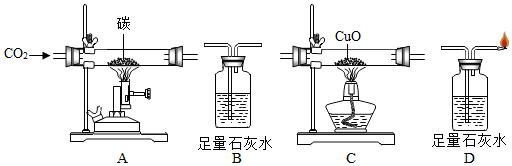
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com