
(3分)食醋是一种能增强食品酸味的常用调味剂,其主要成分为醋酸(CH3COOH),它与我们的生活密切相关。请你根据所学知识,回答下列问题:
(1)食醋有酸味,因为醋酸的水溶液显____ .(填“酸性“、“中性”或“碱性”)。
(2)醋酸中,质量分数最大的元素是____ 元素。
(3)生活中,可用食醋软化鱼骨和鸡蛋壳,因为醋酸能与它们的主要成分反应,生成醋酸钙、二氧化碳和水。由此可推知鱼骨、鸡蛋壳主要成分是(填化学式)____ ____ 。
 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:初中化学 来源: 题型:填空题
胃酸分泌过多的人不宜多饮碳酸型饮料,因为其中溶有较多的CO2气体,该气体能与水反应生成一种酸,该酸的化学式是 ① ,其水溶液能使紫色石蕊试液变 ② 色;常用胃舒平(主要成分含氢氧化铝)治疗胃酸过多症,该反应的化学方程式为 ③ ;向敞口放置一段时间后部分变质的烧碱溶液中滴加稀盐酸,产生的现象是 ④ ,所发生的反应中,不属于中和反应的化学方程式 ⑤ 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(7分)已知A是酸,其浓溶液有脱水性;B为氮肥,C为钾肥,
D为白色不溶于水的固体。它们之间的转化关系如下图: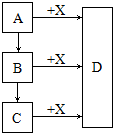
(1)D的名称是 。
(2)A和X反应的化学方程式为: 。
(3)B转化为C的化学方程式为: 。
(4)实验室稀释A的浓溶液操作方法:
。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(4分)(1)配制10%的盐酸的步骤有:①稀释 ②计算 ③装瓶并贴标签 ④量取浓盐酸和水.其正确的顺序为 (填序号).
(2)配制氢氧化钠溶液时,需要的玻璃仪器有量筒、烧杯、滴管及 。
(3)用配得的氢氧化钠溶液与待测的硫酸溶液反应,实验过程中
溶液的pH变化曲线如图所示: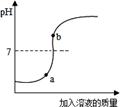
a点对应的溶液呈 (填“酸性”、“碱性”或“中性”);
b点对应的溶液中的溶质为 (写化学式).
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一。镀锌层犹如铁皮的保护层,这层膜的厚度是判断镀层质量的重要指标。某研究性学习小组为了测定镀锌铁皮镀锌层的厚度,设计了下面的实验方案。
(1)讨论:在铁皮表面镀锌是为了 。(填字母)
a 锌没有铁活泼,镀在铁的表面可防止生锈
b 锌比铁活泼,并且在空气中容易形成致密的氧化膜,防止生锈
(2)甲同学的方案是:如图1,将镀锌铁皮浸泡在盐酸中,先用盐酸将镀锌铁皮表面的锌反应掉,通过测量因产生气体而形成差量计算出锌的质量,然后再计算得到锌层的厚度。但是乙同学回顾起上课时老师演示的“用足量盐酸除铁锈”的实验现象,马上对甲同学的方案的可行性提出了异议,乙同学的理由是 。
(3)乙同学查阅资料:ZnCl2、FeCl2都能与NaOH溶液反应,生成难溶于水Zn(OH)2和
Fe(OH)2,而Zn(OH)2既可以溶于酸也可以溶于碱,Fe(OH)2则只能溶于酸,于是设计了如下方案:
步骤②中加入足量氢氧化钠的目的是 。
(4)丙同学设计通过测量镀锌铁皮与酸反应产生气体的体积来计算锌层的厚度,他设计了如图2所示装置。其中仪器A中盛放的是镀锌铁皮,仪器B中盛放的是稀硫酸。
①选择用稀硫酸而不用浓盐酸的原因是 。
②检查量气装置气密性:连接好装置,关闭弹簧夹,从量气管注水,若观察到 ,说明该量气装置气密性良好。
③若分液漏斗上方不连接导管a,则测出气体体积会 (选填“偏小”、“偏大”或“没有影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(9分)纳米碳酸钙是一种重要的无机化工产品,下图是某厂生产纳米碳酸钙的工艺流程。
请回答下列问题:
(1)请完成并配平该工艺中生成CaCO3固体的反应方程式:
CaCl2+_________+CO2=CaCO3↓+__________+H2O
(2)若在实验室中进行该实验,操作l的名称是___________,使用到的非玻璃实验用品有_________、________。
(3)上述过程制得的碳酸钙粗品表面可能含有的可溶性杂质有___________(写一种化学式即可)。操作2为:_________、检验和干燥,检验操作中选用的试剂为____________(选择序号)。 ①NH4Cl溶液 ②AgNO3溶液 ③CaCl2溶液 ④Ba(NO3)溶液
(4)上述流程中的副产品可用作__________________________________。(写一种用途)
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
请根据要求填空:
(1)胃液里含有的酸 (填化学式)
(2)“金银铜铁锡”俗称五金,其中金属活动性最强的是 ;在某黄金样品上滴加稀盐酸后,看到样品表面有气泡产生,说明此样品为 (选填“真”或“假”)黄金
(3)人体内最多的金属元素是 (填化学式)
(4)金属能导电,一般导线都是用金属 制成
(5)金属冶炼通常使矿石中金属元素转变为_______(填“化合”或“游离”)态。
(6)酸有多种分类方法,如下表格:
| 一元酸 | 酸根 | 二元酸 | 酸根 |
| HCl | Cl | H2SO4 | SO4 |
| HNO3 | NO3 | H2CO3 | CO3 |
| CH3COOH | CH3COO | | |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
亚硫酸钠(化学式为Na2SO3)溶液能和BaCl2溶液反应,生成亚硫酸钡白色沉淀,亚硫酸钡能溶于盐酸中,以上反应的化学方程式如下:
Na2SO3+BaCl2=BaSO3↓+2NaCl;BaSO3+2HCl=BaCl2+SO2↑+H2O,实验室中的亚硫酸钠若保存不当就容易与空气中的氧气反应生成硫酸钠。为了检验储存的一瓶亚硫酸钠是否变质,取少量亚硫酸钠样品配制成溶液,再取溶液少许,滴入氯化钡,然后再滴入硝酸,
(1)若亚硫酸钠未变质观察到的现象是 ;
(2)若亚硫酸钠部分变质,观察到的现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com