
【题目】如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,下列结论错误的是( )
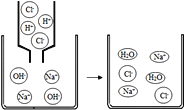
A. 反应结束时溶液的pH=7
B. 反应前后元素的种类没有变化
C. 反应后溶液中存在的粒子只有Na+和Cl﹣
D. 该反应的实质是H+和OH﹣结合生成水
科目:初中化学 来源: 题型:
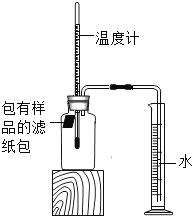
【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表。
序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
1 | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
3 | …… | 100 | 70 | 约480 |
(1)实验①和②说明NaCl可以_____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是_____。
(4)已知含碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成_____。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_____(小数点后保留1位)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据所学知识并结合下列仪器,回答有关问题
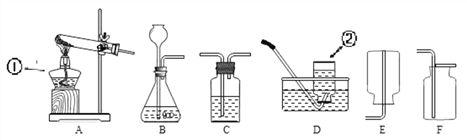
(1)写出对应仪器的名称:①_________________ ②___________________。
(2)实验室加热高锰酸钾制取并收集一瓶较纯净的氧气,应选择的装置组合是_____(填序号),该反应的化学方程式______;若收集的氧气不纯,其可能原因有________(填一种即可)。
(3)常见气体发生装置除了固体加热型和固液不加热型之外,还有固液加热型等。下图G装置是用铜和浓硫酸反应的实验装置
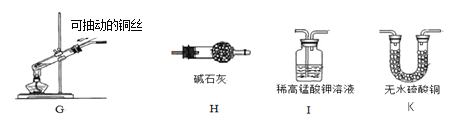
①反应原理:Cu + 2H2SO4(浓) △______+ SO2↑ + 2H2O
②G装置中将铜丝设计为可抽动,是为了控制___________________。
③生成物中的SO2是一种空气污染物,它会导致_____________(填一种空气污染名称)。
④若要验证生成物中有SO2和水蒸气,请从H、I、K中选择合适的装置序号填空:G →____→___________→尾气处理装置。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据所给的信息和标志,判断下列说法错误的是
A | B | C | D |
《淮南万毕术》中记载,曾青得铁则化为铜。 | 《梦溪笔谈》中记载,鄜、延境内有石油,旧说“高奴县出脂水”,即此也。 |
|
|
是现代湿法冶金的先驱 | 这里的石油指的是一种油脂 | 看到有该标志的丢弃物,应远离并报警 | 贴有该标志的物品是可回收物 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定标有质量分数为32%的盐酸的实际质量分数,小明实验时先在烧杯中加入20 g 40%的氢氧化钠溶液,再逐滴加入该盐酸,测定出加入盐酸的质量与烧杯中溶液pH的关系如图。
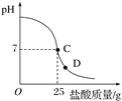
(1)所用氢氧化钠溶液中溶质的质量为_____g。
(2)请认真看清上图信息后回答以下问题。
①当滴加盐酸到C点时,所消耗的盐酸中溶质的质量是多少?_____。
②该盐酸的实际质量分数是多少?(保留到0.1%)_____。
③导致盐酸溶液的溶质质量分数改变的原因是_____。
④当滴加盐酸到图像中D点时,烧杯中溶液的溶质是_____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某化学兴趣小组。设计的金属活动性顺序的探究实验。
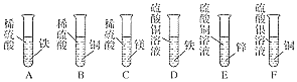
(1)上述实验中,有气泡生成的是________(填写装置序号)。
(2)试管F中出现的实验现象是______________。
(3)上述实验能否证明镁、锌、铁、铜、银五种金属的活动性强弱?____请说明理由_____。
(4)我国古代“湿法炼铜”就是利用了试管D中的反应原理,请写出该反应的化学方程式:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源。
(1)海水制盐。从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加稍过量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发。正确的操作顺序是 (填字母)。加Na2CO3溶液的作用是除去 。
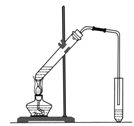
(2)海水淡化。下图是一个简易的蒸馏法淡化海水的装置。证明得到的水是淡水的方法是 。
(3)海水制镁。从海水中提取金属镁的过程如下图所示:
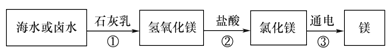
在上述转化过程中发生中和反应的是 (填反应顺序号)。海水中本身就含有氯化镁,则①、②两步的作用是 。
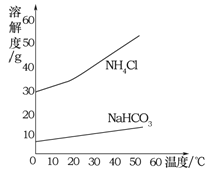
(4)海水“制碱”。氨碱法制纯碱是先通过化学反应生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱。
①氨碱法制纯碱中生成NaHCO3和NH4Cl的化学方程式为 ;
②反应中生成NaHCO3和NH4Cl的质量比为84∶53.5,NaHCO3和NH4Cl的溶解度曲线如图所示。请分析NaHCO3结晶析出而NH4Cl没有结晶析出的原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、X、Y、Z六种初中常见的物质,甲、乙、丙含有相同的金属元素,甲常作为补钙剂;X的固体常用于人工降雨,Y、Z都显碱性,但不属于同类别物质,Z俗称为纯碱。(“﹣”表示物质之间发生反应,“→”表示物质之间能一步转化)回答下列问题:
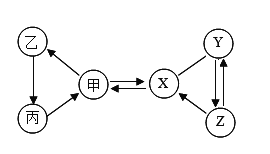
(1)Z的化学式为_____。
(2)写出乙→丙反应的化学方程式:_____,反应类型为_____(填基本反应类型),该反应过程中_____(填“放热”或“吸热”)
(3)①写出X+Y反应的化学方程式:_____。②写出Z→Y的反应的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰好完全反应时:
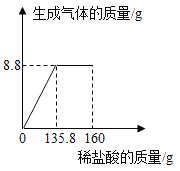
(1)产生的二氧化碳的质量是 克。
(2)此时所得到的溶液中溶质的质量分数(写出必要的计算过程,结果保留到0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com