


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 (2013?启东市模拟)(1)粉笔是一种常用的教学用品,已知其主要成分中含有钙元素.小强和小雯同学一起探究粉笔的组成.
(2013?启东市模拟)(1)粉笔是一种常用的教学用品,已知其主要成分中含有钙元素.小强和小雯同学一起探究粉笔的组成.| 实验操作 | 实验现象 | 结论 | |
| 甲 | 取样于试管中,滴加 石蕊 石蕊 试液 |
试液变红 | 有盐酸 |
| 乙 | 取样于试管中,逐滴滴加碳酸钠溶液至过量 | 有气泡生产 有气泡生产 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
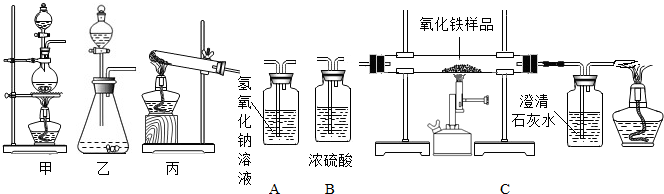
| ||
| △ |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| Cl- | NO3- | CO32- | HCO3- | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 溶 | 溶 | 不溶 | 溶 |
| 实验步骤 | 实验现象 | 结论 |
| 实验1:取少量该白色固体于试管中加热,并将产生的气体通入澄清石灰水中. | 澄清石灰水 变浑浊 变浑浊 . |
证明原白色固体中含有碳酸氢钠. |
| 实验2:取实验1中剩余固体于另一支试管中,加入少量稀盐酸并通入澄清石灰水中. | 有气泡产生,澄清石灰水变浑浊. | 证明原白色固体中还含有碳酸钠 |

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水,充分振荡 | 固体粉末全部溶解 固体粉末全部溶解 |
猜想a、c不成立,猜想b成立. |

| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. |
装置的气密性良好. | |
| ② | 打开分液漏斗活塞,向A 装置中缓慢加入稀盐酸. |
A装置中观察到的现象有 有大量的气泡产生 有大量的气泡产生 ,C装置中有气泡出现. |
A装置中发生反应的化学方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ ;C装置作用是 除去没有反应的二氧化碳 除去没有反应的二氧化碳 . |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com