
【题目】用化学用语表示:
(1)4个钠离子______。
(2)2个氮原子______。
(3)7个二氧化硫分子______。
(4)二氧化氮中氮元素为+4价______。
(5)氢氧化钙______。
(6)三个硫酸根离子______。
【答案】4Na+ 2N 7SO2 ![]() Ca(OH)2 3SO42-
Ca(OH)2 3SO42-
【解析】
(1)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故4个钠离子可表示为:4Na+。
(2)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氮原子表示为:2N。
(3)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则7个二氧化硫分子可表示为:7SO2。
(4)由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后,故二氧化氮中氮元素为+4价可表示为:![]() 。
。
(5)氢氧化钙中钙元素显+2价,氢氧根显-1价,其化学式为:Ca(OH)2。
(6)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其元素符号前加上相应的数字,故3个硫酸根离子可表示为:3SO42-。


科目:初中化学 来源: 题型:
【题目】某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
(1)小红同学用下图总结了 NaOH 的四条化学性质(即 NaOH 与四类物质能够发生化学反应)。
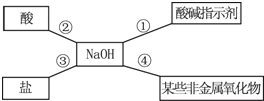
依据上图反应④说明 NaOH 必须密封保存,否则在空气中要变质,KOH 也有类似的化学性质。某研究性学习小组发现一瓶未密封的 KOH 固体,对其成分提出以下假设,并完成了实验探究。
假设一:只含 KOH;
假设二:___________;
假设三:只含 K2CO3 。
Ⅰ.成分中可能含有 K2CO3的原因是_____________。
Ⅱ.进一步探究的过程如下:
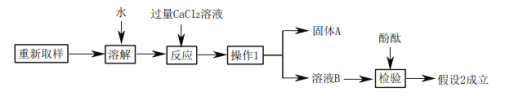
①操作1的名称是________。
②溶液 B 中含有的阳离子有______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室中常见装置,回答下列问题。
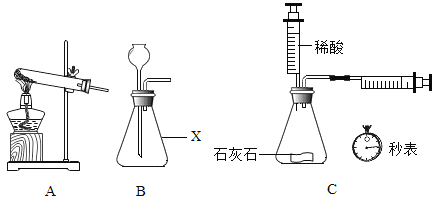
(1)仪器X的名称是______________。
(2)实验室用氯酸钾制取O2应选用的发生装置是______ ( 填字母序号)反应的化学方程式是______________,该反应属于______________(填反应类型)。
(3)利用图C装置探究不同地区石灰石与酸反应的剧烈程度。选用规格大小相同的不同地区的石灰石与等体积稀酸反应,从酸的角度说明还需要控制的变量有______________,实验时通过测定_____________来比较。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高纯硅是制造计算机芯片的重要材料。如图是元素周期表中硅元素的相关信息及原子结构示意图,下列说法正确的是( )
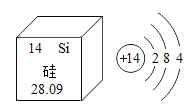
A. 硅元素属于金属元素
B. 硅原子核外有4个电子
C. 硅的相对原子质量为28.09
D. 硅原子在化学反应中易失电子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某品牌粉笔的成分为碳酸钙、硫酸钙,可能含有少量氧化钙。取37g干燥的粉笔研磨成粉末,加入足量稀盐酸,充分反应后得到8.8g气体。将反应后的固液混合物蒸干,测得其中钙元素质量为13.5g。(说明:硫酸钙与稀盐酸不反应)
(1)根据化学方程式计算37g粉笔中碳酸钙的质量。
(2)推断该粉笔中是否含有氧化钙。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验室里,小玲与同学欲用如图所示装置(气密性良好)和药品制取初中化学常见气体并验证其有关性质。
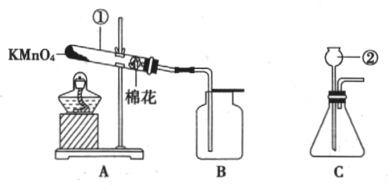
(1)写出图中标有序号的仪器名称:①___________,②____________。
(2)点燃A中的酒精灯制取并收集氧气,反应的化学方程式为____________。
(3)将点燃的蜡烛放入集满氧气的集气瓶中,可观察到____________且瓶壁上有水雾出现,证明蜡烛燃烧有水生成。接着,将蜡烛从集气瓶中取出,____________(填实验步骤和现象),证明蜡烛燃烧还生成了二氧化碳。
(4)小玲同学发现装置C可用于制取二氧化碳,反应的化学方程式为____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化镁(MgO2)是一种镁精细化工产品。在医疗上可用来治疗消化不良、胃酸过多等疾病。在环境保护方面,过氧化镁可用来处理地下水污染的土壤。还可以用于牙膏,对牙齿有漂白和防过敏的作用。某化学兴趣小组对过氧化镁的性质和制备等进行了以下研究。
一.过氧化镁的性质
(1)过氧化镁(其中氧元素的化合价为____)是一种白色的粉末,其外观与物理性质与氧化镁相似。化学性质不够稳定,不溶于水,但逐渐的被分解放出氧气。
过氧化镁有强氧化性,常温下比较稳定,但是加热时会分解生成氧气和氧化镁。请下出该反应的化学方程式________。
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl=MgCl2+H2O2同时温度升高,说明该反应热量__________(填“放出”或“吸收”)。
二.过氧化镁的制备
下图是利用碱式碳酸镁(Mg2(OH)2CO3)和30%的过氧化氢溶液来制取过氧化镁。
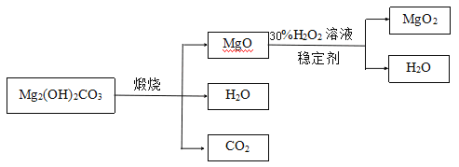
(资料)①碱式碳酸镁与碳酸镁有相似的化学性质,能与稀盐酸反应产生二氧化碳②氧化镁与过氧化氢反应放出大量的热
(3)检测煅烧过程碱式碳酸镁完全分解的方法是_________(写出具体的操作和现象);上述生产过程加入稳定的剂的作用是________。
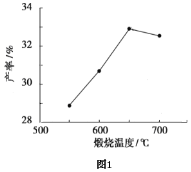
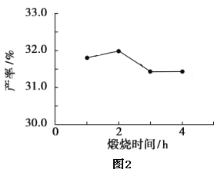
(4)用上述碱式碳酸镁在550、600、650及700℃下煅烧一定的时间生成氧化镁。用上述条件制备的氧化镁分别与30%双氧水反应合成过氧化镁产率(见图1和图2)。
碱式碳酸镁煅烧的温度适宜控制在________℃,煅烧的时间适宜控制在______h。
(5)结果在适宜的温度和时间下,碱式碳酸镁能完全分解,并且得到的氧化镁颗粒表面积最大,能与30%过氧化氢充分反应,所以产率高。推测700℃时,产率明显降低的可能的原因____。
三.过氧化镁产品纯度检测
在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑),以下是该小组进行纯度检测的实验装置和实验步骤。

①检查装置气密性,装入药品(样品质量为0.7g),调节刻度管使左右两边液面相平,刻度管度数为10.0mL。
②打开分液漏斗开关,待瓶中无气泡产生时,关闭开关。
③再次调节刻度管使左右两边液面相平,刻度管度数为122mL。
(6)稀盐酸中放入的少量硫酸铜溶液目的是__________。
(7)根据上面实验数据计算样品中过氧化镁的质量分数__________(写出具体的计算过程,实验条件下O2密度为1.429g/L)。
(8)该小组同学所测得质量分数比实际结果偏大,你觉得可能的原因是(_______)
A 生成的氧气有少量溶于水 B 未等装置冷却到室温就开始读数
C 杂质与盐酸反应能产生少量的气体 D 滴入的稀盐酸占了一部分气体的体积
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据图1、2所示信息,回答相关问题。
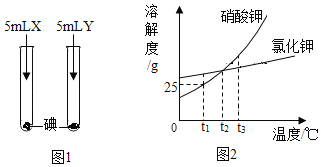
(1)图1所示实验,X、Y分别是水和汽油中的一种,实验中观察到:加入X后固体消失并得到棕色溶液,加入Y后固体未消失,则X是_______________,由实验可知,物质的溶解性与________________有关。
(2)图2为硝酸钾和氯化钾的溶解度曲线,则:
①t1°C时,硝酸钾的溶解度为_________________________。
②t1°C时,将20g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为__________________。
③t2°C时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是_________________________。
④将t3°C时硝酸钾、氧化钾的饱和溶液各100g 分别蒸发10g水,然后降温至t2°C,过滤,得到硝酸钾溶液a和氯化钾溶液b。对于溶液a和溶液b,下列说法正确的是__________________________。
A 都是饱和溶液
B 溶质质量a=b
C 溶质的质量分数a=b
D 溶液质量a<b
E 溶剂质量a<b
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧化铜与稀盐酸发生反应时,容器中溶液总质量随时间的变化由线如图所示。下列说法正确的是
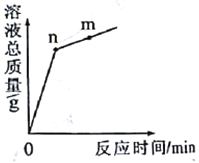
A. 该实验是将氧化铜逐渐加入稀盐酸中
B. n点和m点对应溶液中铜元素质量不相等
C. n点和m点对应溶液蒸发结晶后得到的固体成分相同
D. 该曲线不能反映溶液中溶剂质量随时间的变化关系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com