解:(1)根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,可推断化学方程式为:Cu+2H
2SO
4(浓)

CuSO
4+2H
2O+X↑中X的化学式为SO
2;
(2)因为是二氧化碳和氢气反应,所以生成物中碳原子、氢原子和氧原子的个数比应该是1:2:2,因此该物质是甲酸(CH
2O
2);
(3)氢氧化钙常用作建筑材料,因为氢氧化钙吸收二氧化碳会变成坚固的碳酸钙;
(4)碳酸氢钠显碱性可以和胃酸反应,反应的化学方程式为NaHCO
3+HCl=NaCl+H
2O+CO
2↑;
(5)高温下氢气与四氯化硅(SiCl
4)反应生成高纯度的硅和盐酸,反应的化学方程式为2H
2+SiCl
4
Si+4HCl.
故答案为:(1)SO
2;(2)甲酸;(3)碳酸钙;(4)NaHCO
3+HCl=NaCl+H
2O+CO
2↑;(5)2H
2+SiCl
4
Si+4HCl.
分析:(1)根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,进行解答.
(2)根据“二氧化碳和氢气反应,只生成一种产物”可判断所生成的有机物中C、H、O元素的原子个数比应与反应物中C、H、O元素的原子个数相同;
(3)根据氢氧化钙的性质进行解答;
(4)根据碳酸氢钠显碱性可以和酸反应进行解答;
(5)根据高温下氢气与四氯化硅(SiCl
4)反应生成高纯度的硅进行解答.
点评:本题主要考查质量守恒定律、物质的性质和用途,物质具有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的,难度不大.

 CuSO4+______↑.+2H2O
CuSO4+______↑.+2H2O CuSO4+2H2O+X↑中X的化学式为SO2;
CuSO4+2H2O+X↑中X的化学式为SO2; Si+4HCl.
Si+4HCl. Si+4HCl.
Si+4HCl.

 CuSO4+ +2H2O
CuSO4+ +2H2O 
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O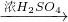 CuSO4
CuSO4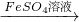 方案三:Cu
方案三:Cu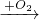 CuO
CuO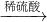 CuSO4
CuSO4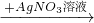 Cu(NO3)2
Cu(NO3)2 Cu(OH)2
Cu(OH)2 CuSO4
CuSO4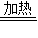 CuSO4+ ↑.+2H2O
CuSO4+ ↑.+2H2O