
 经过蒸发结晶,小组同学提纯了氯化钠.
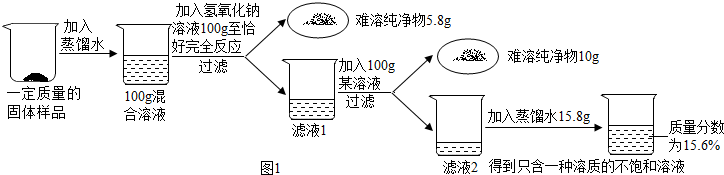
经过蒸发结晶,小组同学提纯了氯化钠.分析 根据题干提供的信息结合数据进行分析解答,氯化镁能与氢氧化钠反应生成氢氧化镁沉淀和氯化钠;溶液稀释前后溶质质量不变;根据标签的内容填写即可.
解答 解:(1)氢氧化钠能与氯化镁反应生成氢氧化镁沉淀和氯化钠,故填:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;
(2)除去氯化钙溶液,则加入碳酸钠溶液,碳酸钠能与氯化钙反应生成碳酸钙沉淀和氯化钠,生成的10g沉淀是碳酸钙,设氯化钙的质量为x,生成氯化钠的质量为z
CaCl2+Na2CO3═CaCO3↓+2NaCl
111 100 117
x 10g z
$\frac{111}{100}=\frac{x}{10g}$;
故填:$\frac{111}{100}=\frac{x}{10g}$;x=11.1g $\frac{100}{117}=\frac{10g}{z}$ z=11.7g
(3)设氢氧化钠的质量为y,则有:
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
80 58
y 5.8g
$\frac{80}{58}=\frac{y}{5.8g}$ y=8g
$\frac{8g}{20%}$=40g,
故加水的质量为:100g-40g=60g,故水的体积为60mL,故填:60;
(4)所加碳酸钠的质量为y
CaCl2+Na2CO3═CaCO3↓+2NaCl
106 100
y 10g
$\frac{106}{100}=\frac{y}{10g}$ y=10.6g
碳酸钠的质量分数为:$\frac{10.6g}{100g}×100%$=10.6%
故填: .
.
(5)设氯化镁的质量为a,生成氯化钠的质量为b,则有
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
95 58 117
a 5.8g b
$\frac{95}{58}=\frac{a}{5.8g}$ a=9.5g $\frac{58}{117}=\frac{5.8g}{b}$ b=11.7g
最后所得溶液的质量为:100g+100g+100g+15.8g-5.8g-10g=300g,故氯化钠的质量为:300g×15.6g=46.8g,故原有氯化钠的质量为:46.8g-11.7g-11.7g=23.4g;
故氯化镁、氯化钙、氯化钠质量比为:9.5g:11.1g:23.4g=95:111:234,故填:95:111:234;
(6)44kg氯化钠样品中含有氯化钠的质量为:44kg×$\frac{23.4g}{9.5g+11.1g+23.4g}$=23.4kg,设生成氢氧化钠的质量为c
NaCl--NaOH
58.5 40
23.4kg c
$\frac{58.5}{40}=\frac{23.4kg}{c}$ c=16kg
则含杂质20%的烧碱的质量为:16kg÷(1-20%)=20kg,故填:20kg.
点评 本题考查的是常见物质的成分以及根据化学方程式的计算的知识,完成此题,可以依据已有的知识进行.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
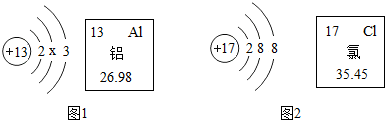
| A. | 该物质属于有机物 | B. | 该物质的相对分子质量为282 | ||
| C. | 一个青蒿素分子里含40个原子 | D. | 该物质中碳元素的质量分数最大 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 能溶于水,水溶液显酸性 | |
| B. | 易溶于水,密度比空气大 | |
| C. | 能溶于水,有毒,能使人窒息而死 | |
| D. | 在某些反应中可作氧化剂,具有氧化性 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 提倡步行、騎自行车等“低碳”出行方式 | |
| B. | 通过加髙烟囱排除放工业废气 | |
| C. | 鼓励用农作物秸秆做燃料 | |
| D. | 施用大量的化肥和农药以提高农作物产量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  向饱和KNO3溶液中加入KNO3 | |
| B. | 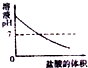 向NaOH溶液中滴加盐酸至过量 | |
| C. |  向CuCl2和HCl的混合溶液中加入加量NaOH溶液 | |
| D. |  向两份同体积和同质量分数的HCl溶液中分别加入足量的铁粉和镁粉 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用水鉴别硫酸铜固体和氢氧化钠固体 | |
| B. | 用带火星的木条检验二氧化碳 | |
| C. | 用肥皂水区别硬水和软水 | |
| D. | 用过滤的方法除去黄河水中的泥沙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com