
为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20 g,逐滴加入氢氧化钡溶液30 g,同时用pH计测定并记录反应过程中混合溶液pH的变化情况(如图所示)。过滤后得滤液47.67 g。请你通过计算 ,求出氢氧化钡溶液的溶质质量分数。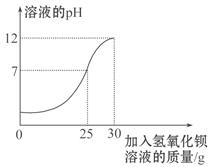
科目:初中化学 来源: 题型:计算题
(3分)氮气是制备含氮化合物的一种重要物质。工业上可在碱性溶液中,通过电解的方法实现由N2制取NH3,反应的化学方程式为:2N2 + 6H2O 通电4NH3 + 3O2。计算生产136t NH3所需N2的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
过氧化氢溶液长期保存会自然分解,使溶液的溶质质量分数减小。小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定其溶质质量分数,他们取该溶液51 g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示。则: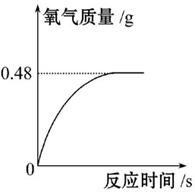
(1)完全反应后生成氧气的质量为 。
(2)计算该过氧化氢溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某钢铁厂需要测定一批生锈较严重的废钢材的锈蚀程度(假定该废钢成分为铁、氧化铁和杂质,杂质不溶于水不发生任何反应,而硫酸先与氧化铁反应),取该样品28g加入一洁净的烧杯中,再将足量的250克稀硫酸平均分为5次加入到烧杯中,获得实验数据如下:
| 稀硫酸质量(单位/g) | 50 | 50 | 50 | 50 | 50 |
| 烧杯内剩余物质总质量(单位/g) | 78 | 128 | 178 | 227.8 | 277.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
黄铜是铜、锌合金,它可用来制造机器、电器零件及日用品。为测定某黄铜样品中铜的质量分数,现取10 g该样品粉碎,加入到50 g稀硫酸中,恰好完全反应,测得剩余固体质量为3.5 g。计算:
(1)黄铜样品中铜的质量分数。
(2)稀硫酸中溶质的质量分数。
(3)由此得到启示是:在使用黄铜制品时应注意 。(合理即可)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
我国早在春秋战国时期,就开始生产和使用铁器。某化学小组到钢铁厂做社会调查,将不同质量的生铁样品(假定其中只含铁和碳两种单质)分别放入5只烧杯中,各加入189.2 g质量分数相同的稀硫酸进行实验,实验数据见下表:
| | 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ |
| 加入生铁样品 的质量/g | 3.0 | 6.0 | 9.0 | 12.4 | 14.0 |
| 充分反应后 生成气体 的质量/g | 0.1 | M | 0.3 | 0.4 | 0.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源,反应的化学方程式为:LiH + H2O="LiOH" + H2↑。计算80 g氢化锂与足量的水反应生成氢气的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为测定某MgSO4溶液的溶质质量分数,化学小组同学取MgSO4溶液100g,向其中加入一定溶质质量分数的NaOH溶液80g,二者恰好完全反应,生成沉淀5.8g.
请计算:
(1)该MgSO4溶液的溶质质量分数是多少?
(2)反应后所得溶液的质量是多少克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(8分)某环保小组监测到一工厂排放的废水中含有H2SO4和CuSO4 。为了测定废水中CuSO4的质量分数,该小组取了100g废水,逐滴加入10%的NaOH溶液至过量。测得生成Cu(OH)2沉淀质量与所加NaOH溶液质量关系如下图所示。 
(1)与H2SO4反应的NaOH溶液质量为 g;100g废水中H2SO4的质量为 g。
(2)计算废水中CuSO4的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com