
| A. | NaOH H2SO4 BaCl2 | B. | HNO3 KNO3 K2SO4 | ||
| C. | NaOH CuSO4 NaCl | D. | Na2SO4 FeCl3 KCl |
分析 若物质之间相互交换成分,能结合成沉淀的则不能得到透明的溶液;本题还要注意能得到无色透明溶液,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:物质加到水中得到无色澄清溶液,说明彼此之间不能生成沉淀,且不存在有色离子.
A、BaCl2和H2SO4生成硫酸钡沉淀,溶液变浑浊,故选项错误;
B、三者之间不反应,符合无色透明的要求,故选项正确;
C、NaOH与CuSO4反应生成氢氧化铜沉淀,溶液变浑浊,故选项错误;
D、三者之间不反应,但FeCl3溶于水呈棕黄色,故选项错误;
故选B.
点评 本题难度不是很大,对于能否得到无色透明的溶液,要注意彼此之间不能生成沉淀,还要注意特定离子的颜色.


科目:初中化学 来源: 题型:推断题
| 非金属元素 | Si | P | S | Cl | |
| 最高价含氧酸 | 名称 | (偏)硅酸 | 磷酸 | 硫酸 | 高氯酸 |
| 化学式 | H2SiO3 | H3PO4 | H2SO4 | HClO4 | |
| 酸性 | 弱 | 中强 | 强 | 强 | |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 A、B、C、D、E是初中化学常见的不同类别物质(单质、氧化物、酸、碱和盐),它们之间相互关系如图(“→”表示反应转化关系,“-”表示相互之间能反应,部分反应物、生成物以及反应条件省略).若往D、E两种溶液中分别滴入紫色石蕊试液,溶液均显蓝色;D与E两种溶液混合有白色沉淀产生;C与E的溶液反应有气泡产生,该气体能使澄清石灰水变浑浊.请回答下列问题:
A、B、C、D、E是初中化学常见的不同类别物质(单质、氧化物、酸、碱和盐),它们之间相互关系如图(“→”表示反应转化关系,“-”表示相互之间能反应,部分反应物、生成物以及反应条件省略).若往D、E两种溶液中分别滴入紫色石蕊试液,溶液均显蓝色;D与E两种溶液混合有白色沉淀产生;C与E的溶液反应有气泡产生,该气体能使澄清石灰水变浑浊.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 木材或纸张着火,用水灭火 | |
| B. | 天然气泄漏,立即打开排气扇通风换气 | |
| C. | 用纯碱代替洗涤剂洗碗 | |
| D. | 印刷厂的碱性废水,加入适量的硫酸中和 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
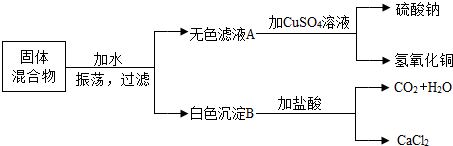
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 漳州小吃手抓面,制作时要用发到大树碱,大树碱的主要成分是K2CO3.为了测定大树碱中K2CO3的质量分数,小文同学进行了如下实验;
漳州小吃手抓面,制作时要用发到大树碱,大树碱的主要成分是K2CO3.为了测定大树碱中K2CO3的质量分数,小文同学进行了如下实验;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com