
| A. |  | |
| B. |  | |
| C. | 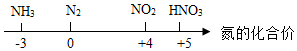 | |
| D. |  |
分析 A.根据气体的密度来分析;
B.根据化合物中元素质量分数的计算方法来分析;
C.根据元素化合价的计算方法来分析;
D.根据相对分子质量的计算方法来分析.
解答 解:A.氧气的密度比空气略大,故错误;
B.观察四种物质的化学式可知:FeS2中一个铁原子相当于对应4个氧原子;Fe2O3中一个铁原子对应$\frac{3}{2}$个氧原子;Fe3O4中一个铁原子对应$\frac{4}{3}$个氧原子;FeO中一个铁原子对应1个氧原子;铁元素的含量由低到高为:FeS2、Fe2O3、Fe3O4、FeO,故正确;
C.氨气中,氢元素显+1价,则氮元素显-3价;氮气中,氮元素显0价;二氧化氮中,氧元素显-2价,则其中氮元素显+4价;硝酸中,氢元素显+1价,氧元素显-2价,则其中氮元素显+5价,故正确;
D.CH4的相对分子质量为12+1×4=16;C2H2的相对分子质量为12×2+1×2=26;CO的相对分子质量为12+16=28;CO2的相对分子质量为12+16×2=44,故正确.
故选A.
点评 明确气体的密度、元素的化合价计算方法、相对分子质量的计算方法以及化合物中元素质量分数的比较方法是解题的关键.


科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滴入适量 FeCl3 溶液,溶液变黄,但无沉淀生成 | |
| B. | 滴入几滴酚酞试液,酚酞试液不变色 | |
| C. | 测得反应后溶液中 Na+与 Cl-的个数比为 1:1 | |
| D. | 滴入适量 AgNO3溶液和稀硝酸,观察到有白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2Fe+6HCl═2FeCl3+3H2↑ | B. | 2NaOH+K2CO3═2KOH+Na2CO3 | ||
| C. | C+O2 $\frac{\underline{\;点燃\;}}{\;}$ CO | D. | CO+CuO $\frac{\underline{\;\;△\;\;}}{\;}$CO2+Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com