
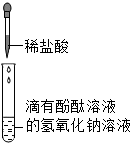
 (1)某同学进行如图实验,证明酸碱发生反应的现象为:试管中溶液由红色变为无色,发生反应的化学方程式为NaOH+HCl=NaCl+H2O.实验后溶液的PH=2,该溶液中含有的溶质有NaCl和HCl(写化学式).
(1)某同学进行如图实验,证明酸碱发生反应的现象为:试管中溶液由红色变为无色,发生反应的化学方程式为NaOH+HCl=NaCl+H2O.实验后溶液的PH=2,该溶液中含有的溶质有NaCl和HCl(写化学式).分析 (1)根据酸碱中和以及酸碱指示剂遇酸、碱的变色情况和溶液的pH与溶液的酸碱性之间的关系来分析解答.
(2)①铁在点燃的条件下能和氧气反应,生成高温熔融物四氧化三铁,所以经常在瓶底放一些水或者细沙,以防炸裂瓶底.工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,写出反应的化学方程式即可;
②把生锈的铁钉放到酸中,表面的铁锈先与酸反应,当铁锈反应完后,铁继续与酸反应.欲证明Cl-的存在,可以利用Ag+来检验.
解答 解:(1)氢氧化钠溶液能使无色酚酞试液变红色,滴入稀盐酸后,氢氧化钠与盐酸发生中和反应生成氯化钠和水,当滴加的盐酸恰好将氢氧化钠完全中和,溶液呈中性,颜色变为无色;若溶液的pH=2,则说明滴加的盐酸过量,溶液中的溶质分别为氯化氢、酚酞、氯化钠.
故答案是:红;NaOH+HCl=NaCl+H2O;NaCl和HCl;
(2)①铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成一种黑色固体四氧化三铁,其反应的化学方程式是3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,为防止铁丝燃烧生成的高温熔融物溅落瓶底使集气瓶破裂,常采取的措施是预先在集气瓶底部放一些水或少量沙子;工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
故答案是:铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成一种黑色固体;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;预先在集气瓶底部放一些水或少量沙子;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
②假设生锈的铁钉插入足量的稀硫酸中,铁锈与硫酸反应,生成硫酸铁与水,所以溶液变为黄色.铁锈反应完后露出铁钉,铁钉与硫酸反应,生成氢气,故有气泡产生.
涉及到的化学反应方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;Fe+H2SO4═FeSO4+H2↑.要证明反应后的滤液中含有Cl-,可以在滤液中滴加 AgNO3溶液,Cl-+Ag+=AgCl↓,若出现 白色沉淀,说明滤液中含有Cl-.
故答案是:Fe+H2SO4═FeSO4+H2↑;AgNO3;白色沉淀.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
| 观察或测定的量 | 需要控制的实验条件 | 实验步骤 | 实验结果与结论 |
| 时间 | 1分钟 | 2分钟 | 3分钟 | 4分钟 | 5分钟 | 6分钟 |
| H2的体积 | 3.1mL | 19.8mL | 28.6mL | 35.2mL | 41.0mL | 45.8mL |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 区分真金和假金(铜锌合金) | 用硫酸铝溶液鉴别 |
| B | 除去硫酸亚铁溶液中含有的硫酸铜 | 加足量的铁粉,过滤 |
| C | 除去CO2中的CO气体 | 在氧气中点燃 |
| D | 除去氯化钠溶液中的碳酸钠溶液 | 加入足量稀盐酸,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na+、H+、Cl-、HCO3- | B. | Na+、K+、NO3-、Cl- | ||
| C. | H+、Na+、OH-、SO42- | D. | Ag+、Ca2+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com