
| A. | H+ Ba2+ NO3- SO42- | B. | H+ NO3- Cl- Ca2+ | ||
| C. | K+ Mg2+ NO3- Cl- | D. | K+ Na+ Mg2+ SO42- |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
 生活中处处有化学.
生活中处处有化学.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 括号中为杂质 | 除杂试剂或方法 |
| A | 氢氧化钠溶液(碳酸钠) | 氯化钙溶液 |
| B | 二氧化碳(氯化氢) | 氢氧化钠溶液 |
| C | 碳酸亚铁溶液(碳酸铜) | 锌 |
| D | 氧化钙(碳酸钙) | 高温煅烧 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
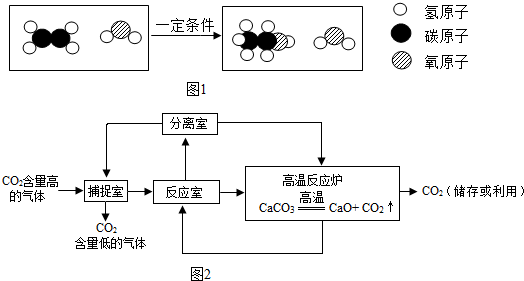
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 促进植物的呼吸作用 | B. | 加速植物的光合作用 | ||
| C. | 增加植物生长所需的微量元素 | D. | 代替碳铵等作氮肥使用 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 两瓶酸的质量都减小 | B. | 两瓶酸的质量都增大 | ||
| C. | 两瓶酸的溶质质量分数都减小 | D. | 两瓶酸的溶质质量分数都增大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| (a)取少量样品溶于水,加入 过量的氯化钙溶液; | 有白色沉淀产生 | 该反应的化学方程式为 Na2CO3+CaCl2═CaCO3↓+2NaCl |
| (b)静置,向将上述反应后的混合液过滤,取滤液加入酚酞试液. | 溶液变红色 | 证明猜想Ⅱ成立 |

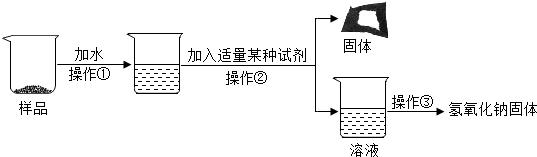
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 合成纤维使得衣料的种类更加丰富,美化了人类的生活 | |
| B. | 化肥的施用使农作物的产量成倍增长,对环境有益无害 | |
| C. | 化学合成药物拯救了很多人的生命 | |
| D. | 滥用食品添加剂对人体有害 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com