将过量的Na
2CO
3溶液滴入到CuSO
4溶液中得到蓝绿色固体.某研究性学习小组对蓝绿色固体的成分进行了如下探究.
【提出假设】
猜想Ⅰ:固体为【CuCO
3,理由是
(用化学方程式表示).
猜想Ⅱ:固体为Cu(OH)
2,理由是Na
2CO
3溶液呈
(填“酸”或“碱”)性.
猜想Ⅲ:固体为CuCO
3和Cu (OH)
2混合物.
【查阅资料】如下:
1、Cu(OH)
2和CuCO
3晶体均不带结晶水.
2、Cu(OH)
2、CuCO
3受热易分解,Cu(OH)
2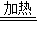
CuO+H
2O,CuCO
3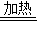
H
2O+CO
2 ↑.
3、无水硫酸铜白色固体,吸水后显蓝色.
【成分探究】
(1)固体的获取:
①将反应后的固、液混合物经
、洗涤、低温烘干得蓝绿色固体.
②判断固体已洗净,可以选用的试剂是
.
A.稀盐酸 B.Na
2CO
3 C.BaCl
2溶液
③低温烘干蓝绿色固体的原因
.
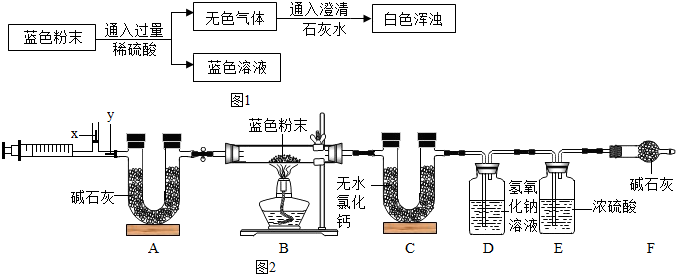
(2)甲同学用图1所示方案,探究固体的成分,并得到下列现象:

①图1中无色气体为
,所以猜想Ⅱ不成立.
②通过测定蓝色溶液的pH,可以判断稀盐酸是否过量.pH测定的方法是
;
③上述实验方案所能得出的结论是一定含有
,方案的不足之处是
.
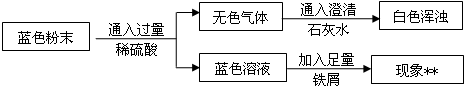
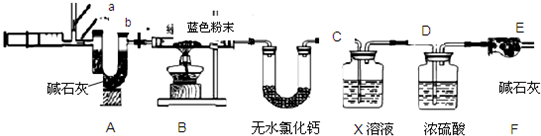
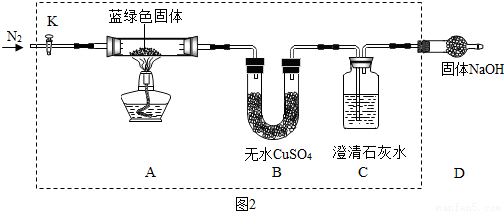
(3)乙同学实验方案如图2所示,
①若观察到B中现象为
,C中现象为
时,猜想Ⅲ是正确的;
②如果要确定固体成分中CuCO
3和Cu (OH)
2的质量比,则还需进行的主要实验操作为
.

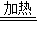 CuO+H2O,CuCO3
CuO+H2O,CuCO3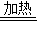 H2O+CO2 ↑.
H2O+CO2 ↑.