
【题目】用化学用语填空:
(1镁 ;(2)2个氮气分子 ;
(3)5个硫酸根离子 ;(4)甲烷 ;
(5)地壳中含量最多的元素 ;(6)氢氧化铝中铝元素显+3价 。
【答案】(1)Mg(2)2N2(3)5SO42-(4)CH4(5)O(6)![]()
【解析】
试题分析:(1)元素符号的书写是:一个字母组成要大写,两个字母组成的一大二小。故镁元素表示为Mg;
(2)化学式前面加数字表示的是分子数目,故2个氮分子表示为2N2;
(3)根据离子的表示方法:在表示该离子的元素符号或原子团的右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,由于1个硫酸根离子带2个单位负电荷,故可表示为SO42-,5个硫酸根离子就在其前再加5,故表示为5SO42-;
(4)一个甲烷分子是由1个碳原子和4个氢原子构成的,故甲烷表示为CH4;
(5)地壳中元素含量排在前四位的是:O、Si、Al、Fe ,含量最多的元素是O;
(6)根据化合价的表示方法:在其化学式中该元素的正上方用正负号和数字表示,且正负号在前,数字在后,则氢氧化铝中铝元素为+3价表示为![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】人类生活生产离不开金属,不仅因为其物理性能优良,还与化学性质密切相关。


(1)钛被称为“21世纪金属”,呈灰色,能在氮气中燃烧,熔点高.钛和钛合金是新型的结构材料,主要用于航天和航海工业.上述描述中属于钛化学性质的是 。
(2)某小组用图所示装置对铁生锈的条件进行探究.4min后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是 。
(3)工业生产常用10%的稀盐酸来除铁锈,写出除锈的化学反应方程式 。
(4)在金属活动顺序表中,金属位置越靠前,越容易失去电子.Ca、Mg、K三种金属失去电子能力由强到弱的顺序是 ,如图是三种原子的结构示意图,据此推测金属失去电子能力的强弱除与最外层电子数有关外,还可能与 有关。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国具有较丰富的煤炭资源,煤制取乙二醇的产业化发展是煤综合利用的方向.煤制取乙二醇的流程示意图为:

(1)煤属于___________(填“可再生”或“不可再生”)能源;
(2)合成气具有还原性,写出CO还原氧化铜的化学方程式:______________,该化学反应中属于还原剂的物质是________________.
(3)合成制取乙二醇的化学反应方程式为:2CO+3H2 =催化剂 = C2H6O2,该化学反应的基本类型是___________;从得氧失氧的角度分析,该反应也是氧化还原反应,其中属于氧化剂的物质是_______________.
(4)根据对(2)与(3)的分析,你对CO的性质有什么新的认识?________________.
(5)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质.仅用合成气为原料不可能得到的物质是________________(填字母序号).
a.草酸(HOOCCOOH) b.甲醇(CH3OH) c.尿素[CO(NH2)2].
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂综合加工海水的主要步骤如图所示.
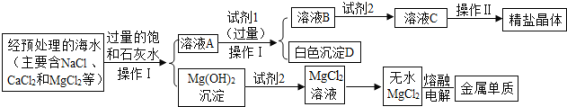
请根据图示回答下列问题:
(1)操作I的名称是_______________。
(2)试剂1是___________________(写化学式,下同),白色沉淀D是____________。
(3)溶液B中含有的溶质是_________________。向溶液B加入试剂2后,在溶液中可观察到_____________的现象。
(4)在熔融状态下电解无水氯化镁会产生一种金属单质和一种双原子分子的气体单质,该反应的化学方程式是_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氮化镁是一种应用范围非常广泛的无机化合物,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物,制备特殊的陶瓷材料等。某校化学研究小组用镁与氮气反应制备氮化镁(Mg3N2),并用实验方法测定氮化镁的纯度。

I.制备氮化镁
【查阅资料】
①(NH4)2SO4+2NaNO2![]() 2N2↑+Na2SO4+4H2O,该反应为放热反应。
2N2↑+Na2SO4+4H2O,该反应为放热反应。
②饱和硫酸亚铁溶液能吸收氧气;稀硫酸能吸收氨气。
③在常温下或温度不高的条件下镁几乎与水不反应。
【实验】
制备氮化镁的装置示意图如下
(1)D装置的作用是______________,G装置的作用是______________。
(2)E装置中发生反应的化学方程式为____________________________。
(3)实验时先进行_____________(选填“A”或“E”)处加热,理由是________________。
II.测定氮化镁的含量
氮化镁是浅黄色粉末,极易与水反应生成Mg(OH)2沉淀和NH3,反应的化学方程式为______________,氮化镁(Mg3N2)中氮元素的化合价是______________。
【定性分析】,
步骤一:取少量氮化镁样品于试管中加足量蒸馏水,试管底部有沉淀生成,试管口闻到有刺激性气味的气体生成。
步骤二:弃去上层清液,加入稀盐酸,观察到沉淀全溶且冒气泡。该步骤中产生气泡的化学方程式为______________________。
【定量测定】按下图实验装置进行实验
 :
:
(4)取氮化镁样品16g进行实验,I装置增重3.4g,求该样品中氮化镁的质量分数(请写出计算过程)。
(5)球形干燥管的作用是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关实验现象的描述正确的是
A.打开盛浓盐酸的瓶塞有白烟生成
B.氢氧化钠溶液中滴加硫酸铜溶液有蓝色沉淀生成
C.黄色pH试纸条沾到碱液变红色
D.光亮铁丝在氧气中燃烧,火星四射,生成四氧化三铁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸镁晶须(MgCO3·nH2O,n = 1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域。为测定碳酸镁晶须中n的值,学习小组设计了如下装置并进行了3次实验:(不考虑稀盐酸挥发)
【查阅资料】:
a、碳酸镁晶须受热分解,生成3种氧化物;
b、相对分子质量:[Mr(MgCO3)∶84、Mr(H2O)∶18、Mr(MgO)∶40、Mr(CO2)∶44]
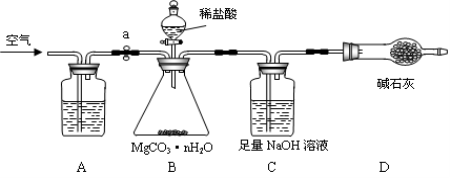
【实验步骤】
①
②准确称取3.45g MgCO3·nH2O放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,称量C装置的质量;
④关闭弹簧夹a,打开分液漏斗活塞,缓缓滴入稀盐酸至不再产生气体为止;
⑤打开弹簧夹a, ;
⑥准确称量C装置的质量(如右表);
⑦重复上述步骤;
⑧根据数据进行计算。
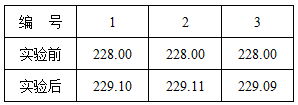
【实验分析及数据处理】
(1)A装置中盛放的溶液是 ,其目的是
(2)D装置的作用是 ;
(3)计算碳酸镁晶须中的n值: (要有计算过程)
【实验反思】
(4)实验结果与理论值有偏差,可以在B、C增加一个 装置以减少误差;
(5)下列选项中,会造成实验结果偏大的是 ;偏小的是 ;
①反应结束后,没有通空气;
②称量C装置前,没有通空气;
③没有A装置;
④没有D装置;
(6)为精确测定n的值,在老师指导下,小组同学称取13.8 g MgCO3·nH2O进行热重分析,并绘制出如图所示的热重曲线示意图。则:
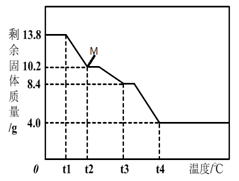
①t2℃时,剩余固体为 (填化学式);
②最终剩余的4.0 g物质是 (填化学式);
③碳酸镁晶须完全分解的化学方程式为: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是氢气在氯气中燃烧生成氯化氢的微观模拟图,请回答下列问题:
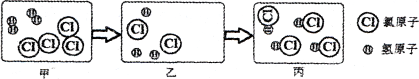
(1)乙图还没画完,请你将乙图补充完整,使该模拟图符合质量守恒定律。
(2)由图示可以得出,在化学变化中,发生变化的是____________(填“分子”或“原子”);
(3)甲到乙的微观实质是:在点燃条件下,氢分子分成氢原子,氯分子分成氯原子,则乙到丙变化的实质是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com