
| A. | 蛋白质、糖类都属于有机物 | B. | 人体缺钙易引起甲状腺肿大 | ||
| C. | 糖类由C、H、O三种元素组成 | D. | 脂肪是维持生命活动的备用能源 |
分析 A、根据有机物的定义判断;
B、根据钙的生理功能判断;
C、根据糖类的元素构成分析;
D、根据脂肪是人体的备用能源分析判断.
解答 解:A、有机物是指含碳的化合物(碳的氧化物、碳酸、碳酸盐除外),蛋白质和糖类符合定义,故A正确;
B、人体缺钙易引起骨质疏松,故B错误;
C、糖类由C、H、O三种元素组成,故C正确;
D、脂肪是维持生命活动的备用能源,故D正确.
故选B.
点评 在生活水平不断提高的今天,人们把健康饮食的问题提到了生活的日程上,因而对六大营养素的考查也成了中考热点之一,特别是六大营养素包括的种类、生理功能、食物来源、缺乏症,摄入时的注意事项等内容,虽然试题难度小,但出现频度高,要引起高度重视.


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 一包白色固体样品中可能含有Na2SO4、Na2CO3、NaCl中的一种或几种,为测定其成分,现进行如下实验:①取样品3.54g,加入适量水使其完全溶解;②先后逐滴加入BaCl2溶液、稀硝酸,产生沉淀的质量与时间的关系如图所示:
一包白色固体样品中可能含有Na2SO4、Na2CO3、NaCl中的一种或几种,为测定其成分,现进行如下实验:①取样品3.54g,加入适量水使其完全溶解;②先后逐滴加入BaCl2溶液、稀硝酸,产生沉淀的质量与时间的关系如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
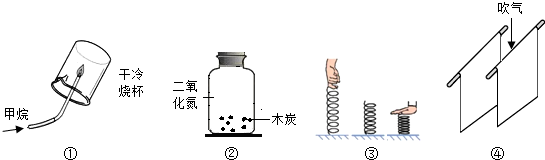
| A. | 图①:烧杯内壁有水珠生成,说明甲烷中含有氢元素 | |
| B. | 图②:瓶中红棕色逐渐褪去,说明木炭具有吸附性 | |
| C. | 图③:用等大的力拉伸和压缩弹簧,弹簧形状不同--力的作用效果与作用方向有关 | |
| D. | 图④:向两张纸的中间吹气,两张纸向中间靠拢,是因为中间的空气流速大,压强大 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
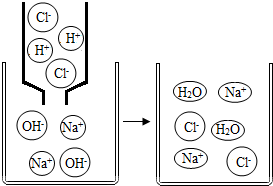 化学是研究物质的组成、结构、性质及变化规律的科学.
化学是研究物质的组成、结构、性质及变化规律的科学.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
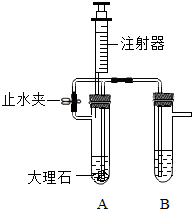 甲、乙、丙、丁四种常见物质,由碳、氢、氧、氯、钠、钙6种元素中的2-3种组成.
甲、乙、丙、丁四种常见物质,由碳、氢、氧、氯、钠、钙6种元素中的2-3种组成.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 结论 |
| 难溶物是CaCO3 |
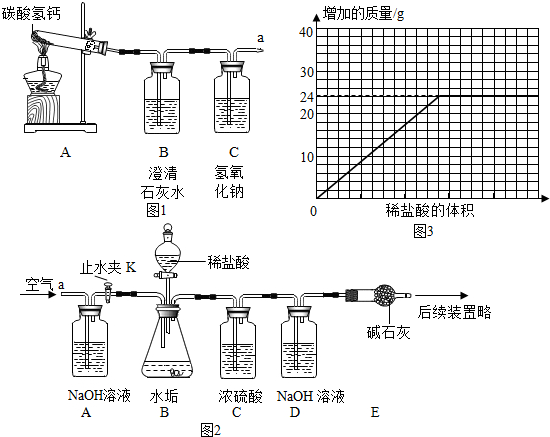
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com