
| OH- | Cl- | CO32- | SO42- | |
| H+ | 溶 | 溶 | 溶 | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| K+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 不 | 微 |


 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:初中化学 来源: 题型:
| 物质名称 | 氯化铝 | 氯化铁 | 氯化铜 |
| 水溶液颜色 | 无色 | 黄色 | 蓝绿色 |
| 实验组别 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | |
| 药品 | 金属单质 | Al | Mg | Zn | Fe | Zn | Al | Cu |
| 氧化物 | CuO | CuO | CuO | CuO | Fe2O3 | Fe2O3 | Fe2O3 | |
| 实验现象 | 取上述粉末状的混合物于密闭试管中高温加热 | 爆炸 | 爆炸 | 变红 | 变红 | 变黑 | 变黑 | 无变化 |
| 冷却后,向上述反应后的固体中加入足量的稀盐酸 | -- | -- | 固体部分溶解,水溶液呈无色 | 固体部分溶解,水溶液呈黄色 | 固体全部溶解,有气体放出,水溶液呈浅绿色 | ? | -- | |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
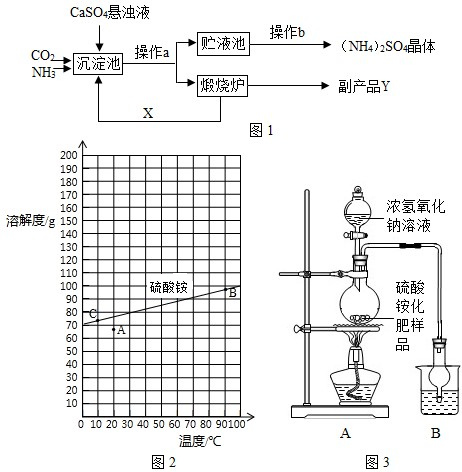
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 溶解度/g | 70.6 | 73 | 75.4 | 78 | 81 | 85 | 88 | ? | 95 | 98 | 103 |
| 指标 项目 |
优等品 | 一等品 | 合格品 |
| 外观 | 白色结晶, 无可见机械杂质 |
无可见机械杂质 | |
| 氮(N)含量 | ≥21.0% | ≥21.0% | ≥20.5% |
查看答案和解析>>
科目:初中化学 来源:2008年湖北省宜昌市中考化学模拟试卷(解析版) 题型:解答题
| OH- | Cl- | CO32- | SO42- | |
| H+ | 溶 | 溶 | 溶 | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| K+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 不 | 微 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com