
【题目】下表是氯化钾和硝酸钾在不同温度下的溶解度。根据表中数据,请回答下列问题:
温度/°C | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 | |
(1)在所示的坐标纸上绘制出氯化钾的溶解度曲线______________。
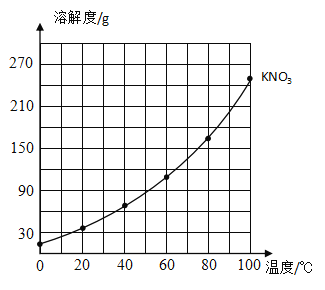
(2)比较两种物质的溶解度曲线,溶解度受温度影响变化较小的是______________,温度大约在___________°C时,两种物质的溶解度大小相等。
(3)60°C时,105g的KNO3饱和溶液中含有的溶质的质量为____________。
(4)40°C时,向烧杯中加入50g水和25gKCl固体,充分溶解后得到的溶液是_____________(填“饱和”或“不饱和”)溶液,其溶质质量分数为_____________(精确到0.1% )。
(5)若KNO3中混有少量的KCl ,提纯KNO3的方法是_____________。
【答案】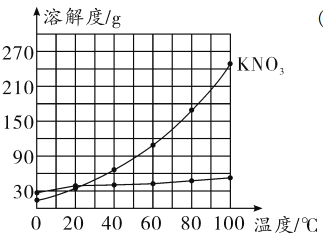 氯化钾 22(其他合理答案均可) 55 g 饱和 28.6% 降温结晶(或冷却热饱和溶液)
氯化钾 22(其他合理答案均可) 55 g 饱和 28.6% 降温结晶(或冷却热饱和溶液)
【解析】
(1)根据表中的数据,在坐标系中找出六个点,然后用平滑的曲线将六个点顺次连接起来,即得到氯化钾的溶解度曲线;
(2)氯化钾的溶解度曲线较硝酸钾的平缓,说明氯化钾的溶解度受温度影响较小,根据曲线可知,大约在22°C时氯化钾和硝酸钾的溶解度相等;
(3)60°C时硝酸钾的溶解度为110g,即210g硝酸钾的饱和溶液中含有的溶质质量为110g,则105g的硝酸钾饱和溶液中含有的溶质的质量为55 g;
(4)40 °C时氯化钾的溶解度为40.0 g,所以该温度下将50g水和25 g氯化钾放入烧杯中充分溶解,所得溶液为饱和溶液,其溶质质量分数为![]() ;
;
(5)硝酸钾和氯化钾的溶解度都随温度升高而增大,但硝酸钾的溶解度受温度影响变化较大,氯化钾的溶解度受温度影响变化不大,所以若硝酸钾中混有少量氯化钾,可通过降温结晶或冷却热饱和溶液的方法提纯硝酸钾。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:初中化学 来源: 题型:
【题目】铁、铜和铝是人类生活中常用的金属。
(1)动物细胞中含量最多的金属元素是_____。
(2)用铜、铝做导线,利用了它们的_____性。
(3)铁锅易生锈,铁生锈的条件是_____。
(4)铜器表面会生成铜锈,其主要成分是碱式碳酸铜[Cu2(OH)2CO3],该物质含有_____种元素,从它的化学式可推知,铜生锈的过程除了与氧气和水有关外,还与空气中的_____有关。
(5)除去铜器表面的铜锈时,加入过量的稀硫酸,生成二氧化碳,同时得到蓝色溶液。若再向上述蓝色溶液中加入足量的铁粉,铁粉与蓝色溶液发生反应的化学方程式为_____。
(6)为了验证锌、铁的金属活动性强弱,小琴同学将锌片和铁片同时插入稀硫酸中,而没有插入硫酸铜溶液中,其原因是_____。
(7)小明买了一种“汽泡爽”的冲调饮料,原料中的柠檬酸和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,3NaHCO3+C6H8O7=C6H5O7Na3+3H2O+3CO2↑.为了探究加水温度对产生气体量的影响,在老师的帮助下,小明采用相同的两套实验装置(如图)分别完成上述实验,在A中加入水,再加入一袋“汽泡爽”,迅速塞紧胶塞。量筒C用于收集A中产生的气体所排出的液体,冷却至室温后读取数据。B中油层的作用是_____。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(11分)(1)实验室用石灰石和稀盐酸制取CO2的原理是 (写化学方程式),可选用下列装置 (填序号)制CO2。设计B装置时使用仪器a的目的是 。
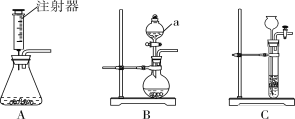
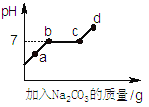
(2)在反应装置的残液中加入Na2CO3溶液,溶液PH变化如图所示(提示:氯化钙溶液呈中性):a点时,溶液中的溶质的化学式是 。bc段溶液pH一直为7的理由是 。滴入Na2CO3溶液的过程中观察到的现象依次是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)氧化钙俗名生石灰,某同学针对氧化钙设计了如下实验方案:
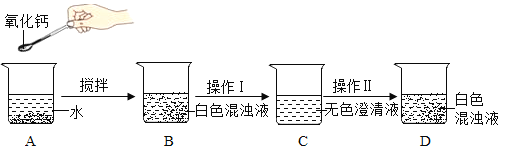
(1)A中发生反应的化学方程式为___________。分离B中难溶物的操作I叫_________。
(2)如果要用实验证明C中不是水而是一种溶液,可以选择下列______(填序号)进行试验。
①稀盐酸 ②酚酞溶液 ③二氧化碳 ④氯化钠溶液
(3)操作II是加入某种物质使无色澄清液出现白色固体,如果加入的是饱和碳酸钠溶液,白色固体的化学式是___________;如果加入的是固体氢氧化钠(全部溶解),白色固体的化学式是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有甲、乙两瓶久置的氢氧化钠固体,某学习小组为了研究其变质情况,进行了如下实验:(电子秤示数单位为g)
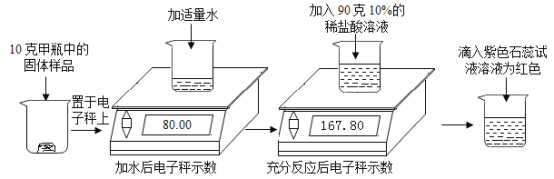
(1)滴入紫色石蕊溶液后溶液为红色,说明反应后溶液呈_____性。
(2)上述实验产生的二氧化碳气体质量为_____g。
(3)计算甲瓶固体样品中碳酸钠的质量分数_____。
(4)某同学另取10 g乙瓶中的固体样品,用100 g 15%的稀硫酸按同样方法进行实验,他认为不管固体样品变质程度如何,稀硫酸加入后,都不需要使用石蕊溶液,请计算说明他做出此判断的原因:根据Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,每106份质量的碳酸钠完全反应需98份的H2SO4,100 g15%的稀硫酸中H2SO4的质量为_____g,所以_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲醚为易燃气体,在爆炸极限范围内遇到火源易发生爆炸。如图是甲醚的微观结构模型,下列有关甲醚的说法正确的是
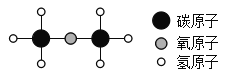
A.甲醚的相对分子质量为46g
B.甲醚完全燃烧生成一氧化碳和水
C.甲醚中碳、氢、氧三种元素的质量比为12:3:8
D.密闭环境中甲醚和空气的混合物在点燃的情况下,一定会发生爆炸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A-F是初中化学常见的6种物质,A~D是不同类别的含氧化合物,A的固态可用于人工降雨,C物质广泛应用于玻璃、造纸、纺织和洗涤剂的生产,E的溶液呈蓝色,E和F反应的生成物为两种沉淀,物质间的关系如图所示(图中部分反应物、生成物已省略,“—”表示反应关系,“→”表示转化关系)。请回答下列问题:
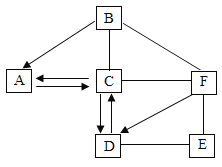
(1)写出C、F的化学式:C_______________;F________________。
(2)物质B属于________(填“酸”、“碱”或“盐”)。
(3)写出D和E反应的化学方程式_____________________________。
(4)写出A→C的化学方程式________________,此反应________(填“属于”或“不属于”)复分解反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是
A.无土裁培的营养液中常含的K2SO4是种复合肥
B.天然河水经吸附沉降过滤消毒杀菌蒸馏净化成生活用的自来水
C.Fe2+和Fe3+都属于铁元素核外电子数不同
D.![]() 和
和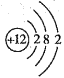 的最外层电子数相同化学性质相似
的最外层电子数相同化学性质相似
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是宝贵的自然资源,日常生活、工农业生产和科学实验都离不开水。蚌埠市自来水公司担负市区生产和生活用水重任。回答下列与水有关的问题:
(1)水是一切生命体生存所必需的物质,爱护水资源,一方面要__________________________________________,另一方面要防止水体污染。
(2)自来水公司的水源一般不是硬水,硬水中含有较多的两种阳离子,是___________________、______________________(用离子符号表示)。区别软水和硬水的办法是取水样, 加入_____, 振荡,若观察到_________________,则是软水。硬水转化为软水,常用的两种方法是_____________________________和__________________________。
(3)如图是自来水厂净水过程示意图。
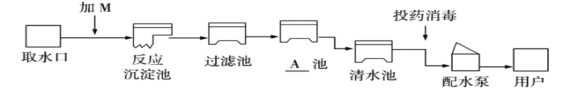
图中M是絮凝剂,常用的絮凝剂名称是___________________________。过滤池可以除去水中的___________________________,在实验室中做过滤实验时常用到的玻璃仪器有(写两种即可)___________________________、___________________________。A池中常投入活性炭,是利用它的__________________________性能,如图是生活中活性炭净水器的示意图:

进水口应选__________________________(填“a”或“b”)。
(4)实验室制蒸馏水时,常在蒸馏烧瓶中加入沸石(或碎瓷片),沸石(或碎瓷片)的作用是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com