
| A. | 用熟石灰和硫酸铜配制波尔多液 | |
| B. | 服用含Mg(OH)2的药物治疗胃酸过多 | |
| C. | 施用熟石灰改良酸性土壤 | |
| D. | 用氨水与工厂排放的含硫酸的废水反应制氮肥 |
分析 中和反应是酸与碱之间生成盐和水的反应,反应物必须是酸和碱,生成物必须是盐和水,据此进行分析判断即可.
解答 解:A、熟石灰与硫酸铜反应生成氢氧化铜沉淀和硫酸钙,不是酸和碱的反应,不是利用了中和反应原理,故选项正确.
B、Mg(OH)2与胃液中的盐酸反应生成氯化镁和水,是酸和碱的反应,是利用了中和反应原理,故选项错误.
C、熟石灰与酸性土壤中的酸反应生成盐和水,是酸和碱的反应,是利用了中和反应原理,故选项错误.
D、氨水与硫酸反应生成硫酸铵和水,是酸和碱的反应,是利用了中和反应原理,故选项错误.
故选A.
点评 本题难度不大,掌握中和反应的特征(反应物必须是酸和碱,生成物必须是盐和水)是正确解答本题的关键.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:初中化学 来源: 题型:解答题
 实验室常用盐酸和石灰石反应制取二氧化碳.
实验室常用盐酸和石灰石反应制取二氧化碳.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 添加剂名称 | 主要化学性质及在体内变化 |
| 碳酸氢钠 | 无毒、弱碱性,易与胃酸反应,加热分解成碳酸钠、水和二氧化碳 |
| 铁 (还原性铁粉) | 比较活泼的金属,能与胃酸反应 |
| 食盐 | 易溶、中性,与硝酸银溶液反应生成白色沉淀 |
| 亚硝酸钠 | 易溶、水溶液显碱性,跟硝酸银反应生成浅黄色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 反应前 | 反应后 |
| E的质量为100.0g | E的质量为102.25g |
| F的质量为50.0g | F的质量为51.1g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
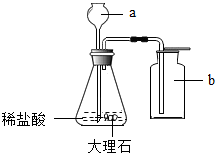 如图是实验室制取二氧化碳的实验装置图,请回答下列问题:
如图是实验室制取二氧化碳的实验装置图,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
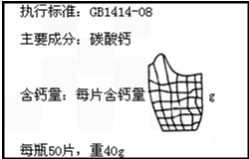 有一瓶钙片,瓶壁上的标签如图所示.
有一瓶钙片,瓶壁上的标签如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com