二氧化碳在化学家的眼里是可以利用的重要资源,只要有合适的条件,可以像发生光合作用那样将二氧化碳转变为所需要的产物.二氧化碳可以为化工合成提供足够的碳元素,既可以减少化工产业对煤和石油的消耗,又可以缓解大气中二氧化碳含量的增加.
(1)二氧化碳和水通过光合作用转变为葡萄糖和氧气的化学方程式为: .
(2)化肥厂用二氧化碳与氨气在一定条件下反应生成尿素[CO(NH2)2]和水的化学方程式为: .
(3)超氧化钾(用X表示)能与二氧化碳反应生成氧气,在载人航天飞机和潜水艇中可用它作制氧剂,供呼吸之用.超氧化钾(X)与二氧化碳反应的化学方程式为:4X+2CO2═2K2CO3+3O2则X的化学式为 .
【答案】
分析:(1)①正确书写葡萄糖的化学式C
6H
12O
6,确定反应物为二氧化碳和水,反应条件为在叶绿体中、光照,生成物为葡萄糖和氧气;
②配平的方法:可以把化学式最复杂的计量数定为“1”,再按“C→H→O”的顺序配平;
(2)由题意知,反应物为二氧化碳与氨气,生成物为尿素[CO(NH
2)
2]和水,根据质量守恒定律,可以书写化学方程式;
(3)根据质量守恒定律:反应前后元素种类不变,原子个数相等,由4X+2CO
2═2K
2CO
3+3O
2,可以推测X的化学式.
解答:解:(1)二氧化碳和水通过光合作用转变为葡萄糖和氧气:确定反应物、生成物、反应条件;选择合适的配平方法,故化学方程式为6CO
2+6H
2O
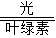
C
6H
12O
6+6O
2.
故答案为:6CO
2+6H
2O
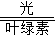
C
6H
12O
6+6O
2.
(2)由题意知,反应物,反应条件,生成物,根据质量守恒定律,故CO
2+2NH
3 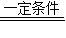
CO(NH
2)
2+H
2O;
故答案为:CO
2+2NH
3 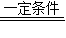
CO(NH
2)
2+H
2O;
(3)根据质量守恒定律:反应前后元素种类不变,原子个数相等,由4X+2CO
2=2K
2CO
3+3O
2,可以推测X的化学式为KO
2.
故答案为:
(1)6CO
2+6H
2O
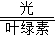
C
6H
12O
6+6O
2.
(2)CO
2+2NH
3 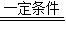
CO(NH
2)
2+H
2O.
(3)KO
2.
点评:根据题目信息,找出反应物和生成物,再利用书写化学方程式的方法及步骤,根据质量守恒定律,正确书写化学方程式.

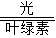 C6H12O6+6O2.
C6H12O6+6O2.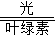 C6H12O6+6O2.
C6H12O6+6O2.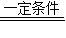 CO(NH2)2+H2O;
CO(NH2)2+H2O;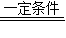 CO(NH2)2+H2O;
CO(NH2)2+H2O;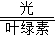 C6H12O6+6O2.
C6H12O6+6O2.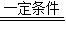 CO(NH2)2+H2O.
CO(NH2)2+H2O.

 阅读快车系列答案
阅读快车系列答案