
����Ŀ��ͼΪ���ֲ�ͬŨ�ȵ�����������Һ���ӦŨ�ȵ����ᷴӦ�����ߡ�
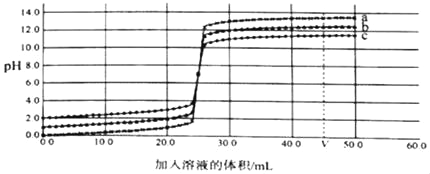
����˵����ȷ���ǣ�������
A. ��a������ʾ��ʵ���У����÷�̪��ָʾ������̪��Һ�ɺ�ɫ��Ϊ��ɫ
B. bʵ��������ǡ����ȫ��Ӧʱ����Һ�к��е�����ֻ��Na+��Cl��
C. ��a��b��c����������ʾ��ʵ���У���Ӧ������ͬ
D. ��a��b��c����������ʾ��ʵ���У���������Ũ��Խ������Һ���ΪVʱ������Һ��pHԽ��
���𰸡�D
��������
A��ͼ����pHֵ�ı仯�Ǵ�С��7��������7����֪ԭ��Һ�����ԣ�Ȼ�ϵļ��������Һ��ʹpH�������������м�������������Һ����a������ʾ��ʵ���У����÷�̪��ָʾ������̪��Һ����ɫ��Ϊ��ɫ����A����
B��bʵ��������ǡ����ȫ��Ӧʱ����Һ�к��е����ӳ�����Na+��Cl��������ˮ���ӣ���B����
C����a��b��c����������ʾ��ʵ���У����ڷ�Ӧ��Ũ�Ȳ�ͬ����Ӧ���ʲ���ͬ����C����
D����ͼ���Կ������������м�������������Һ����a��b��c����������ʾ��ʵ���У�ǡ����ȫ��Ӧ����pH��7ʱ����Ҫ����������Һ�����ȣ������������Ũ��Խ����Ҫ���������������ҺŨ��ҲԽ������Һ���ΪVʱ������������Һ������������Һ��pHԽ��D��ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ��̽��ȼ�յ��������ⶨ�����������ĺ���(����ƿ�ݻ�Ϊ250mL)��ʵ�鲽�����£�

����ͼ����������������ע�����Ļ�����һ��ʱ����ɿ��֣�ע�����Ļ����ָ���ԭλ��
�����п�ȼ�ճ��Ϸ���һС��(����)���ף������������ر�K��
�����ձ��е�������80�����ˮ��
�ܴ�K����ע�����Ļ�����������100mL�����۲�����
��2���Ӻ�Ѹ�ٽ�ע�����Ļ��������ײ����������ر�K���۲�����
��������
�ش��������⣺
(1)����ٵ�ʵ��Ŀ����___________________��
(2)��ʵ���з�����Ӧ�Ļ�ѧ����ʽΪ__________��
(3)����ܹ۲쵽��������__________��
(4)��ʵ���������ˮ��������__________��
(5)����IJ������۲쵽��������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������ⶨ������ʶ��
��ʵ��عˣ���ͼ��ʵ�����ú���ȼ�������Բⶨ����������������װ�á�

��1��д������ȼ�յ����ֱ���ʽ_________������________��ѡ����ϡ��ֽ⡱����Ӧ��
��2��ʵ��ԭ�������ں���ȼ�����Ŀ����е�_____��ʹƿ��ѹǿ______���ձ���ˮ����������ƿ����װ�õ����������ã������淶���ܴ��Բ������Լռ�����������__________��
�������������ʵ�����ϱ�����ȼ�չ����е����������������7% ʱ������������ȼ�գ����ͨ������ʵ�飬�ⶨ���������ֵ���ϴ�
��ʵ��Ľ���
��һ���������ڿ����������ԭ�������ͼʵ��װ�ã��ٴβⶨ����������������װ���б���ʳ��ˮ������̿����������⡣

���������ʵ���������£�

������ƿ���۳�������͵��ܵ������=126.0 mL���ձ���ˮ�����
�����������1����������̷������ӵĻ�ѧ��Ӧ������������������ˮ��Ӧ��������������[Fe(OH)2]��д���÷�Ӧ�����ֱ���ʽ_______��
��2�����ݲ��ʵ�����ݼ��㣺���뼯��ƿ��ˮ�������______mL���Ľ�ʵ����õĿ��������������������_________ (��������ȷ��0.1%)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ�ã���ϴ���������ȶ��ֹ��ܡ����й��ڸ�װ����;��˵������ȷ����_____
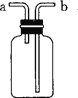
A���������ſ������ռ�CO2�������a�ܽ�
B������ˮ���ռ�H2��ƿ��װ��ˮ�������a�ܽ�
C���������������ƿ��װ��ˮ�������b�ܽ�a�ܽ���Ͳ
D�����ڲ���������ƿ��װˮ��______�ܽӹ�����ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С�ͬѧ��ͨ����ѧʵ����֤�������غ㶨����������������ʵ��̽����
��ʵ����ƣ�����ʵ��Ŀ�ģ�С�ȷ���ԡ���������ͭ��Һ��Ϊ�о�������Ƶ�ʵ��װ�D��ͼ����ʾ��
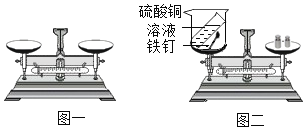
������ʵ�飩
ʵ�鲽�� | ʵ���������¼ | ���ͻ���� |
������ |
| ��ͼһ��ʾ������ƽ����ĸ��ƽ��ƽ���ԭ���� _________�� |
�ڳ������������� | ��¼��������Ϊ5.6g |
|
����������ͭ��Һ���ձ��������� | ��¼��������Ϊ113.2g |
|
����������ʢ������ͭ��Һ���ձ��� | _____________________________________________ | �÷�Ӧ�Ļ�ѧ����ʽΪ__________________________�� |
�ݳ�ַ�Ӧ����ͼ����ʽ�ź�������ҩƷ������ | ��¼��������Ϊ_____________ | �÷�Ӧ���������غ㶨�� |
��������˼����1���������ʵ���Һ�����������ͭ��Һֱ������ͼ��װ���������ʵ�����______������ţ��� A�������� B��ϡ���� C�������� D���Ҵ�
��2��ʵ��������˲�����ձ��еĻ���ϴ�Ӻ����������������Ϊ5.8g�����ʵ��������ͭ������Ϊ___________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס������ֹ�������(�������ᾧˮ)���ܽ��������ͼ��ʾ������˵����ȷ����
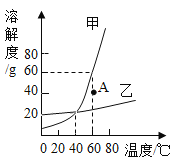
A. �ס������ʶ����ý��½ᾧ��ʹ���ʴ���Һ������
B. 60��ʱ��40g�����ʼ���50gˮ���ܵõ�90g������Һ
C. ͨ��������ʹA��IJ�������Һ��Ϊ������Һ
D. �ֱס������ʱ�����Һ��60�潵��20�棬����������϶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��̽�� ��˫�Ʒ��������ࡢ����塱��������۵���Ҫ�ɷ֡�
���������ϣ���1����������۾�����Ħ���������Լ������ϵȳɷֹ��ɡ�
��2�����õ�Ħ�����м�ϸ������̼���(CaCO3) ��ˮ�Ϲ���(SiO2��nH2O)�ȡ�
��3������������г���̼������⣬�������ʾ�����ϡ���ᷴӦ�������塣
��ʵ��һ��̽��������������������Ƿ���̼��ƣ�
���� | ʵ����� | ʵ������ |
�� |
��ͼ��ʾ��ȡ��ֻ�Թֱܷ��������������Ʒ���ٷֱ��������xϡ��Һ��xϡ��Һ��____________�� | A�Թ��������Ա仯�� B��C�Թ�������ɫ�������ɡ� |
�� | ��B��C�Թ������ɵ���ɫ����ͨ��__________�� | �����____________�� |
ʵ����ۣ� __________ ��
̼�����xϡ��Һ��Ӧ�Ļ�ѧ����ʽΪ___________��
��ʵ������Ƚ���Ʒ��̼��Ƶĺ���
���� | ʵ����� | ʵ������ |
�� | ��װ������ͼװ�ý���ʵ�顣�ֱ�ȡ��������������ƿ�С����ڷ�Һ©���зֱ�����������xϡ��Һ��
| |
�� | ��Һ©��ע��һ����xϡ��Һ��Ȼ��رջ����� | �����ݲ����� |
�� | ���ڷ�Ӧ�������ٴ�Һ©����ע��һ����xϡ��Һ��Ȼ��رջ����� | ���������� |
�� | ������Ӧ��װ�ü�ҩƷ�������������ԱȽ� | ���롰˫�Ʒ����������װ�ü�ҩƷ�����������ڼ������۵�װ�ü�ҩƷ�������� |
ʵ����ۣ�_____________________
����۵������ǣ�_________________��
����˼��
��1�������Ķ�ԭ��װ�úͻ������裬Ҫ�ⶨ������̼��Ƶ�������������Ӧ�ⶨ�������У�_____��
��2��С����Ϊ������õ����ݼ�����������ϴ�����Է��������������______���ƫ����ƫС����û�С�����ԭ����_______��������Ϊû�����ղ����
��3��С����Ϊ��ʵ��ǰ����Ҫ�ⶨװ�õ������ԣ�����˵����ԭ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷Ͼɵ��ͭñ����Cu��Zn����ȡ����ͭ��Cu�������õ�����п��ҺE����Ҫ��������ͼ��ʾ����Ӧ��������ȥ����
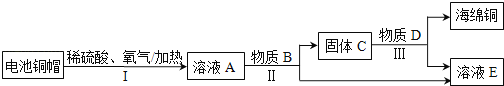
��1������I�лᷢ����2Cu+2H2SO4+O2![]() 2CuSO4+2X��X�Ļ�ѧʽΪ_____��
2CuSO4+2X��X�Ļ�ѧʽΪ_____��
��2�����̢����ȼ������B����ַ�Ӧ���ٽ��з��룮���������������_____�����˸ò������õ��IJ����������ձ�����������_____����������������_____��
��3������D��һ���ᣬ���̢�Ӧ�Ļ�ѧ����ʽΪ_____���жϹ���C�еķ�ͭ���ʱ�����D��Ӧ��ȫ�������ǣ���������Dʱ��_____��
��4��A��E�к�ͭ��п����Ԫ�ص���_____������ĸ��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��KNO3���ܽ�����������˵���������
�¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 |
�ܽ��/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
A. ����ص��ܽ�����¶�Ӱ��仯�ϴ�
B. 60 ��ʱ�������������Һ����������Һ����֮��Ϊ11��21
C. 20 ��ʱ��10 gˮ�м���5 g����س���ܽ���ټ���5 gˮ��ǰ�����ʵ�������������
D. ��������������Ϊ28%���������Һ��60 �潵����20 �棬û�о�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com