
【题目】把一定质量的甲,乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量分数变化如图所示。下列说法中错误的是( )
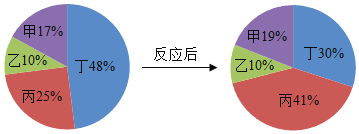
A. 该反应为分解反应B. 乙可能是此反应的催化剂
C. 参加反应的甲、丁的质量之比为9:1D. 丁一定是化合物,甲、丙可能是单质
【答案】C
【解析】
由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数增加了19%-17%=2%,故甲是生成物;乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应;反应后丙的质量分数增加了41%-25%=16%,故是生成物;丁的质量分数减少了48%-30%=18%,丙是反应物。
A、该反应的生成物为甲和丙,反应物是丁,符合“一变多”的特征,属于分解反应,选项A正确,不符合题意;
B、乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应,选项B正确,不符合题意;
C、参加反应的甲、丁的质量之比为2%∶18%=1∶9,选项C错误,符合题意;
D、该反应属于分解反应,丁是分解反应的反应物,一定是化合物,甲、丙是分解反应的生成物,可能是单质,选项D正确,不符合题意。故选C。


科目:初中化学 来源: 题型:
【题目】某地成功处置了一辆满载三氯化磷(PCl3)的车辆泄漏事故.三氯化磷是一种重要的无极工业产品,无色液体、密度1.574g/cm3 (21℃),熔点-112℃,沸点75.5℃,易燃.遇水反应生成亚磷酸(H3PO3)和氯化氢,与有机物接触会着火.下列对三氯化磷的说法错误的是( )
A. ![]() 中磷元素的化合价为
中磷元素的化合价为![]()
B. 运输途中应防雨淋和防高温
C. 运输过程中如果发生燃烧时,可以用水浇灭
D. 三氯化磷与水反应的化学方程式:![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组利用下图所示装置进行相关实验,请你根据下图回答问题:
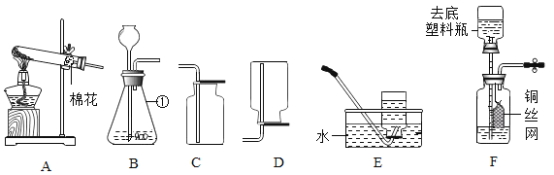
(1)写出标有序号①的仪器名称_______。
(2)实验室用高锰酸钾制取并收集较纯净的氧气可选择的装置组合是_____,写出该反应的化学方程式______。试管口放一团棉花的目的是________。某同学用收集好的氧气做铁丝燃烧实验时发现集气瓶炸裂,原因可能是______。
(3)实验室里检验二氧化碳的方法是_____(用化学方程式表示)。图F是某同学利用塑料瓶和其它用品设计的制取二氧化碳的发生装置,该设计与B装置比较除了废物利用的优点外,请另写一个优点_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年5月我国海域可燃冰(天然气水合物)试采获得成功。2017年6月1日,特朗普宣布美国退出《巴黎协定》,引起国际社会强烈反响,使能源和环境问题再次成为热点。可燃冰是资源量丰富的高效清洁能源,能释放出天然气。
(1)生活中,可以利用天然气(主要成分是甲烷,化学式为CH4)获得热量,甲烷燃烧产物为二氧化碳和水。该反应的化学方程式为____________________________________;
(2)微粒观是化学的重要观念之一。工业上,可以利用甲烷获得氢气,其反应的微观示意图如下:
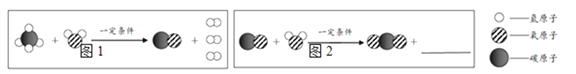
①图1所示反应的化学方程式为 _____________________________ ;
②在图2横线处补全相应微粒的图示 ____________________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用硫铁矿烧渣(主要成分是Fe3O4、Fe2O3等)、煤粉作原料制备FeCO3的主要流程如图:
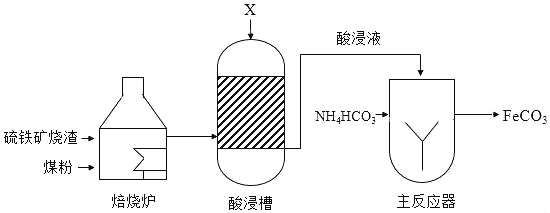
(1)焙烧炉中,发生的主要反应为:
①3C+2O2![]() 2CO+CO2
2CO+CO2
②Fe2O3+CO![]() 2FeO+CO2
2FeO+CO2
③Fe3O4+CO![]() 3FeO+CO2
3FeO+CO2
上述反应中的各物质,碳元素呈现_____种化合价.
(2)酸浸槽中,FeO转化为FeSO4,加入的物质X是_____.
(3)主反应器中,生成FeCO3的反应物为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)实验室用过氧化氢与二氧化锰制取氧气的化学方程式为:______,加入二氧化锰是为了______。
(2)如表是某研究小组探究影响化学反应速率的因素的相关实验数据:(每次实验取用含碳酸钙60%的大理石10g.每次实验盐酸的用量为20mL,大理石中杂质不与盐酸反应)。
实验编号 | 温度/℃ | 大理石规格 | 盐酸的质量分数 | 完全反应的时间/s |
a | 20 | 粗颗粒 | 18.25% | 130 |
b | 粗颗粒 | 9.125% | 205 | |
c | 30 | 粗颗粒 | 18.25% | 63 |
d | 20 | 细颗粒 | 18.25% | 95 |
(实验目的)
①实验a和b探究大理石颗粒大小相同下盐酸的质量分数对该反应速率的影响,则实验b中的温度应该为______。
②实验a和c探究______对该反应速率的影响。
③实验a和______探究大理石颗粒大小对该反应速率的影响。
④根据表格中的数据写出2个与实验目的相对应的实验结论:______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某集团是一家以生产电缆类产品为主的国家大型企业.在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组的四位同学得知这一情况后,围绕“从含铜废料中回收铜”提出了各自的看法.
甲同学根据已学知识,提出了一套回收方案:
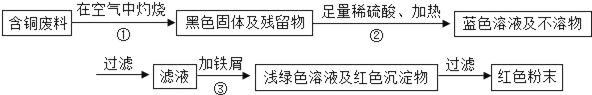
乙同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu+2H2SO4+O22CuSO4+2H2O),于是他提出了另一套方案:
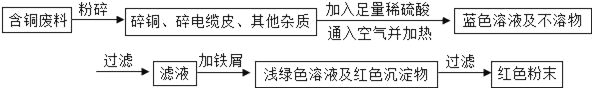
(1)甲方案的①②③三个步骤中,与铜或铜的化合物有关的化学反应方程式分别是:①_____;②_____;③_____.
(2)从环保角度对两套方案的不同部分进行比较,你认为_____(填“甲”或“乙”)的方案更合理.理由是:_____.
(3)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑.你认为丙这么说的道理是:_____.
丁又提出了疑问:“如果铁过量,剩余的铁会混在红色粉末中,该怎么处理呢?”.请提出你的想法:_____.
(4)最后,老师肯定了同学们的积极思考,但同时指出:方案最后一步所得浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益.请写出使“绿矾”结晶的两种可能方法:_____、_____(“绿矾”溶解度随温度升高而增大).如果直接排放掉滤液,不仅造成了浪费,还会_____.
(5)若上述方案所用的稀硫酸溶质质量分数为36.8%,问每1000mL98%的浓硫酸(密度为1.84g/mL)能配制出这种稀硫酸_____g,需水_____mL(水的密度为1.0g/mL).在实验室中稀释浓硫酸时,是如何操作的:_____.
(6)根据乙同学查出的方程式(2Cu+2H2SO4+O2![]() 2CuSO4+2H2O)计算:如果1000mL98%的浓硫酸(密度为1.84g/mL)稀释后全部参加了反应(假设硫酸不和碎电缆皮、其他杂质反应),所能处理的废料中含纯铜____克。(请写出计算过程,结果精确到0.1克)
2CuSO4+2H2O)计算:如果1000mL98%的浓硫酸(密度为1.84g/mL)稀释后全部参加了反应(假设硫酸不和碎电缆皮、其他杂质反应),所能处理的废料中含纯铜____克。(请写出计算过程,结果精确到0.1克)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图A、B、C、D是初中化学中常见的四种物质。其中A为黑色单质,D为紫红色单质。B、C是组成元素相同的两种气态化合物。“![]() ”表示物质间的转化关系(部分反应物,生成物及反应条件省略)请回答:
”表示物质间的转化关系(部分反应物,生成物及反应条件省略)请回答:
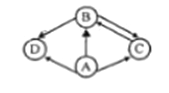
(1)实验室制取C的化学方程式是_________;
(2)B的一种用途_________;
(3)A![]() D反应的化学方程式是_________。
D反应的化学方程式是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是一切生命体生存所必需的物质
(1)木兰溪水中含有许多杂质,可利用吸附、沉淀、过滤、蒸馏等方法净化水,其中净化程度最高的方法是_____;
(2)硬水给生活和生产带来很多麻烦,生活中检验溪水是硬水还是软水可使用_____(写一种试剂),通常可以采用_____的方法来软化硬水。
(3)如图是电解水实验装置。在实验过程中,试管b中产生的气体是_____,请写出水在通电条件下反应的文字表达式:_____,其反应的基本类型为_____。
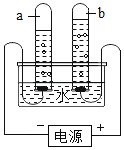
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com