
| 温度/℃ | 0 | 10 | 20 | 30 | |
| 溶 解 度 | NaCl | 35.7 | 35.8 | 36.0 | 36.3 |
| KNO3 | 13.3 | 20..9 | 31.6 | 45.8 | |
| Ca(OH)2 | 0.185 | 0.176 | 0.165 | 0.153 | |
分析 (1)根据氯化钠的溶解度受温度影响变化不大,进行分析解答.
(2)根据氢氧化钙的溶解度随着温度的升高而减小,进行分析判断.
(3)根据10℃时,氯化钠和硝酸钾的溶解度分别是35.8g、20.9g,进行分析解答.
解答 解:(1)氯化钠的溶解度受温度影响变化不大,使氯化钠从其饱和溶液中结晶 出来,最好采用的方法是蒸发结晶.
(2)氢氧化钙的溶解度随着温度的升高而减小,将10℃时的饱和石灰水升温到30℃,氢氧化钙的溶解度减小,有氢氧化钙析出,溶液中溶质的质量将减小.
(3)10℃时,氯化钠和硝酸钾的溶解度分别是35.8g、20.9g,10℃时,在两只烧杯中各加入100g水,然后分别加入30g氯化钠和30g硝酸钾,充分搅拌后,氯化钠能全部溶解,最多只能溶解20.9g硝酸钾,所得溶液中溶质的质量不相等,溶剂的质量相等,则所得两种溶液中溶质的质量分数不相等.
故答案为:(1)蒸发结晶;(2)减小;(3)不相等;所得溶液中溶质的质量不相等,溶剂的质量相等.
点评 本题难度不大,掌握结晶的方法与原理、溶质的质量分数、溶解度的含义等是正确解答本题的关键.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:多选题
| A. | 第一次反应停止,B剩余9g | B. | 第二次反应后,C剩余5g | ||
| C. | 反应中B和C的质量比是3:2 | D. | 反应中A和C的质量比为5:3 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 实验室有一瓶标签被腐蚀的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中配制了8g10%的NaOH溶液,然后往烧杯中滴加盐酸.反应过程中溶液的pH与滴入盐酸的质量关系如图所示.请回答下列问题:
实验室有一瓶标签被腐蚀的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中配制了8g10%的NaOH溶液,然后往烧杯中滴加盐酸.反应过程中溶液的pH与滴入盐酸的质量关系如图所示.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
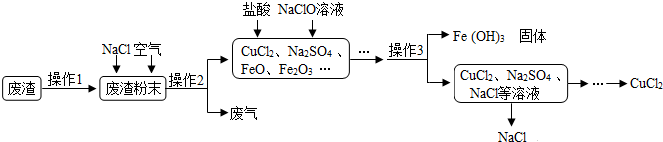
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 3Al3+--3个铝离子 | |
| B. | 2N2--2个氮分子 | |
| C. | CaCl2--氯化钙中钙元素的化合价显+2价 | |
| D. | C60--石墨 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| A | B | C | D | |
| 分类标准 | 金属氧化物 | ② | 盐 | ④ |
| 不属于该类别的物质 | ① | Cu | ③ | H2O |
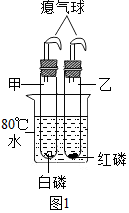
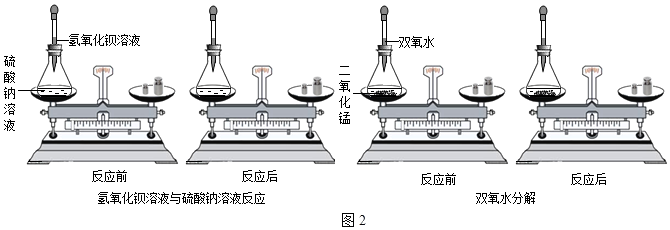
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 取样品粉末,加入适量的水,充分搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣(或氢氧化钙样品)于试管中,加入盐酸 | ①变红色; ②有气泡生成. | ①氢氧化钙还有剩余; ②说明氢氧化钙与二氧化碳反应有碳酸钙生成. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com