填空
(1)在食盐中加入适量的碘酸钾(KIO3),可以有效地预防碘缺乏病.根据碘酸钾的化学式计算:
①KIO3的相对分子质量为______.
②我国规定,食盐加碘的含量为每千克食盐含碘0.035克,相当于每千克食盐含碘酸钾______克.
(2)根据尿素的化学式[CO(NH2)2]计算:
①尿素的相对分子质量为______
②有一不纯的尿素样品,测知含氮元素44.8%,若已知杂质不含氮元素,此化肥的有效成分尿素的质量分数为______.
解:(1)KIO
3的相对分子质量=39+127+16×3=214;
KIO
3中碘(I)元素的质量分数=
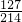
×100%≈59.3%
含碘0.035g的碘酸钾的质量=0.035g÷59.3%≈0.059g
(2)尿素CO(NH
2)
2的相对分子质量=12+16+(14+1×2)×2=60
尿素[CO(NH
2)
2]中氮元素的质量分数为:
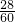
×100%≈46.7%,
尿素的质量分数=44.8%÷46.7%×100%=95.9%
故答案为:(1)214;0.059
(2)60;95.9%
分析:(1)由碘酸钾的化学式KIO
3可知,碘酸钾由K、I、O三种元素组成,其分子含1个K原子、1个I原子和3个O原子;根据碘酸钾的化学式,可计算其相对分子质量、组成元素的质量比、组成元素的质量分数及一定质量的碘酸钾中所含碘元素的质量.
(2)利用尿素的化学式中各原子的原子量计算相对分子质量,物质的质量分数等于氮元素的质量分数与尿素中氮元素质量分数之比.
点评:本题主要考查学生运用化学式进行计算的能力.解题时要注意计算物质中元素原子的个数以便进行正确的计算.

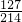 ×100%≈59.3%
×100%≈59.3%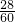 ×100%≈46.7%,
×100%≈46.7%,
