
某大理石样品(所含杂质不溶于水且不与酸反应)与足量的盐酸充分反应,过滤后将绿叶蒸干,冷却后称量所得氯化钙固体,相关实验数据如下图所示(不计损耗):
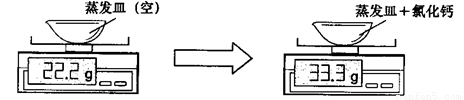
(1)氯化钙的质量为______________g。
(2)计算该大理石样品中碳酸钙的物质的量(根据化学方程式列式计算)。
(1)11.1(2)0.1mol
【解析】(1)据图可知,空的蒸发皿的质量为22.2g,蒸发皿加上氯化钙的质量为33.3g,则氯化钙的质量为33.3g—22.2g=11.1g。所以氯化钙的质量为11.1 g。
(2)已知:氯化钙的质量为11.1 g,未知碳酸钙的物质的量。
解题思路:可根据反应中氯化钙与碳酸钙的关系进行计算。
解:设碳酸钙的物质的量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
1 mol 111g
x 11.1g
1 mol:x=111g:11.1g
x=0.1 mol
答:样品中碳酸钙的物质的量为0.1mol。
考点:托盘天平的计数、根据化学方程式的计算
点评:本题考查的是化学方程式的计算。解题时,要找出题中已知的量;然后根据物质间的关系进行计算。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源:2013年初中毕业升学考试(上海卷)化学(带解析) 题型:问答题
某大理石样品(所含杂质不溶于水且不与酸反应)与足量的盐酸充分反应,过滤后将绿叶蒸干,冷却后称量所得氯化钙固体,相关实验数据如下图所示(不计损耗):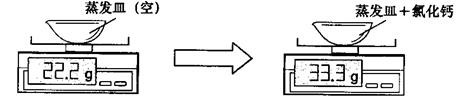
(1)氯化钙的质量为______________g。
(2)计算该大理石样品中碳酸钙的物质的量(根据化学方程式列式计算)。
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源:2013年上海市中考化学试卷(解析版) 题型:解答题
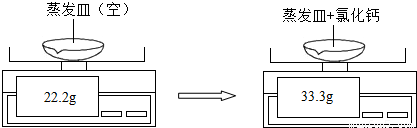
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com