
| 该元素相对原子质量×原子个数 |
| 该物质的相对分子质量 |
| 16×3 |
| 32+16×3 |
| 3 |
| 5 |
| 16×2 |
| 32+16×2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 5 |
| 32 |
| 32+16×3 |
| 2 |
| 5 |
| 32 |
| 32+16×2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 2 |
| 5 |


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:初中化学 来源: 题型:
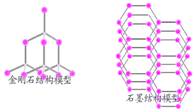
| A、碳原子结构不同 |
| B、石墨含有杂质 |
| C、碳原子的排列方式不同 |
| D、碳元素化合价不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:
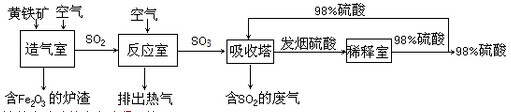
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
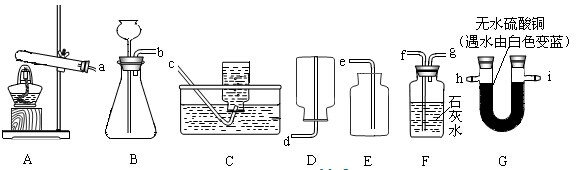
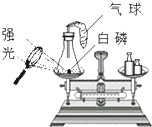 某化学兴趣小组利用如图装置进行质量守恒定律的探究.
某化学兴趣小组利用如图装置进行质量守恒定律的探究.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com