
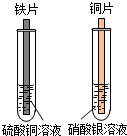
 如图,金属及金属材料在生产、生活中应用广泛.
如图,金属及金属材料在生产、生活中应用广泛.分析 根据铁片和硫酸铜溶液反应生成铜和硫酸亚铁以及铜片和硝酸银溶液生成银和硝酸铜,结合金属的活动性顺序进行解答.
解答 解:①铁片和硫酸铜溶液反应生成铜和硫酸亚铁,所以将铁片插入硫酸铜溶液中,铁片表面的现象是有紫红色的物质生成;
②铜片和硝酸银溶液生成银和硝酸铜,反应的化学方程式是Cu+2AgNO3=Cu(NO3)2+2Ag.此探究实验的目的是探究铁、铜、银三种金属的活动性顺序.
故答案为:①有紫红色的物质生成;②Cu+2AgNO3=Cu(NO3)2+2Ag;探究铁、铜、银三种金属的活动性顺序.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行,注意方程式的书写.


 优加精卷系列答案
优加精卷系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 干冰升华需吸收大量的热,可用于人工降雨 | |
| B. | Ca(OH)2能与酸反应,可用于改良酸性土壤 | |
| C. | 甲醛能使蛋白质变性,可用于食用水产品防腐 | |
| D. | 明矾溶于水能形成吸附性物质,可用于自来水厂净水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 要区分的物质 | 方法一 | 方法二 |
| A | 黄铜和黄金 | 观察颜色 | 在空气中加热 |
| B | 氯化铵和硫酸钾固体 | 加熟石灰研磨 | 加入适量水观察是否溶解 |
| C | 羊毛制品和纯棉制品 | 点燃闻气味 | 观察颜色 |
| D | 稀盐酸和氢氧化钠溶液 | 加入大理石 | 加入硫酸铜溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
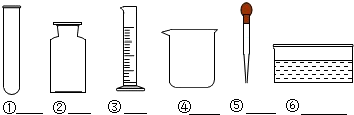
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
| 充分反应后生成气体的质量/g | 0.88 | 1.76 | 2.64 | 3.52 | 3.52 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
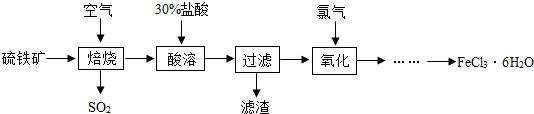
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com