
【题目】用如图实验装置进行探究实验。
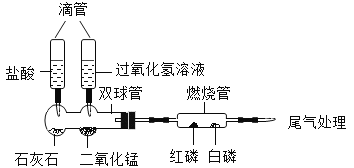
(1)挤压左滴管并微热燃烧管,白磷和红磷均不燃烧,挤压右滴定管并微热烧管,燃烧管中白磷燃烧而红磷不燃烧,由此可说明燃烧需要什么条件?_____
(2)相同质量的磷、铁、镁分别在氧气中完全燃烧,消耗氧气最多的是_____。
【答案】可燃物与氧气接触,温度达到可燃物着火点 磷
【解析】
(1)由图可知挤压左滴管,石灰石与盐酸反应生成二氧化碳气体,微热燃烧管,白磷和红磷均不燃烧,说明燃烧时可燃物需要与氧气接触;挤压右滴定管,过氧化氢在二氧化锰作催化剂的条件下分解生成氧气,微热烧管,燃烧管中白磷燃烧而红磷不燃烧,说明燃烧时温度需要达到可燃物的着火点。
(2)磷、铁、镁在氧气中完全燃烧的化学方程式分别为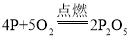 、
、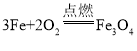 、
、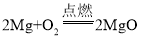 ,由方程式可知每124份质量的磷与160份质量的氧气恰好完全反应,每168份质量的铁与64份质量的氧气恰好完全反应,每48份质量的镁与32份质量的氧气恰好完全反应,则相同质量的磷、铁、镁分别在氧气中完全燃烧,消耗氧气的质量比为
,由方程式可知每124份质量的磷与160份质量的氧气恰好完全反应,每168份质量的铁与64份质量的氧气恰好完全反应,每48份质量的镁与32份质量的氧气恰好完全反应,则相同质量的磷、铁、镁分别在氧气中完全燃烧,消耗氧气的质量比为![]() ,则消耗氧气最多的是磷。
,则消耗氧气最多的是磷。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体也有多种可能吗?”
(猜想)碳与氧化铜反应生成的气体中:①只有CO2;②只有CO;③_____________。
(查阅资料)浸有磷钼酸溶液的氯化钯试纸遇CO2,无变化,但遇到微量CO会立即变成蓝色。
(方案设计)通过上述资料和已有知识,小雨初步设想用浸有磷钼酸溶液的氯化钯试纸和澄清石灰水对碳与氧化铜反应生成的气体进行检验。根据小雨的设想,请你完成填空。
(1)若试纸不变色,澄清石灰水变浑浊,则猜想①成立。
(2)若试纸______,澄清石灰水_______,则猜想②成立。
(3)若试纸______,澄清石灰水_______,则猜想③成立。
(实验验证)经过思考之后,小雨设计了如下图所示的实验装置。
实验步骤:
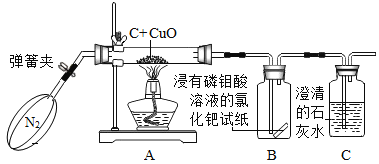
(1)打开弹簧夹,先通一会儿纯净、干燥的N2。
(2)关闭弹簧夹,点燃酒精灯加热。
(结论)小雨通过分析实验现象,确认猜想③是正确的。请你写出装置A中发生反应的化学方程式_______________;_____________;
(反思与评价)该实验开始通一会儿N2的目的是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸和碱作用生成盐和水的反应叫中和反应。某化学兴趣小组同学对“盐酸中和氢氧化钠溶液”的反应进行探究。
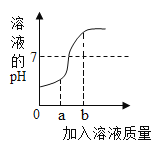
(1)小明在做“盐酸中和氢氧化钠溶液”的实验时,测出反应过程中溶液的pH变化如图所示。
①该反应的化学方程式为:___________________。
②该实验操作是将_________________滴加到另一种溶液中。
③当加入溶液的质量为ag时,所得溶液中的阳离子有(写符号)_______________。
④当加入溶液的质量为bg时,向所得溶液溶液中滴入紫色石蕊试液,紫色石蕊试液变_______色。
(2)小亮在做“盐酸中和氢氧化钠溶液”的实验时,向氢氧化钠溶液里滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度,于是他对所得溶液的酸碱性进行探究。
(探究目的)探究所得溶液的酸碱性。
(提出猜想)所得溶液可能呈酸性,也可能呈____________性,还可能呈碱性。
(实验验证)
实验操作 | 实验现象 | 结论 |
用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡。 | 无色酚酞试液变________色 | 溶液呈碱性 |
无色酚酞试液不变色 | 溶液呈_________。 |
(交流与反思)
①若溶液呈碱性,则溶液中使其呈碱性的离子是_________(写符号)。
②若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入镁条,若有____________现象,则呈酸性;若无明显现象,则呈中性。
方案二:取样,加入一枚表面生锈的铁钉,若观察到铁锈消失、溶液变成黄色,则所取溶液呈酸性,反应的化学方程式为____________;若无明显现象,则呈中性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过阅读和观察模型回答问题:
(1)人类发现二氧化碳经历了多个世纪,下列是其历程中的部分资料。
资料一:1630年,海尔蒙特发现在一些洞穴处,有一种能使燃着的蜡烛熄灭的气体,后来被证实是CO2。
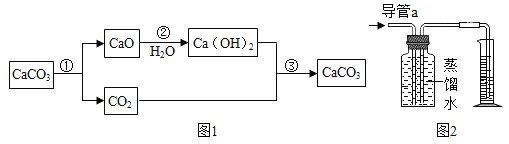
资料二:1754年,布莱克将石灰石煅烧首次制得CO2,并完成如图1所示的物质转化研究。
资料三:1766年,卡文迪许通过实验测得:室温下1体积水大约能溶解1体积二氧化碳气体。
①根据海尔蒙特的发现,可推测二氧化碳的化学性质____________。
②写出布莱克实验中既不是化合反应又不是分解反应的一个方程式___________。
③如图2,在室温下将容积为200毫升的广口瓶注满蒸馏水,通过导管a缓慢通入300毫升CO2.如果卡文迪许的结论是正确的,则在量筒中收集到的水约为_______毫升。
(2)人们常用模型来进行认知,因为这种方式形象直观。图1是水分子和乙炔分子的模型,图2是原子核转变的模型。
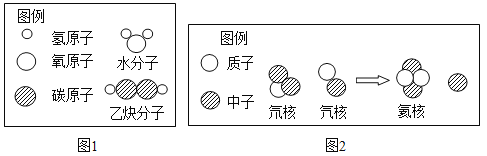
①碳原子和氧原子的画法参照上述图例,请画出“碳和氧气反应生成二氧化碳”的化学反应模型图:________________。
②图1中可作溶剂,对生命活动具有重要作用的物质是___________(写化学式)。乙炔中氢元素的化合价为+1价,请结合模型判断乙炔中碳元素的化合价为______________。
③通过观察氕核和氘核图示,判断氕和氘_________(填是或否)为同种元素,图2是_________(选填“核裂变”或“核聚变”)的示意图。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,有关说法正确的是( )
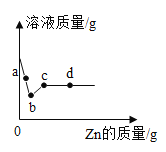
A.a点溶液中的溶质有2种
B.b点得到的固体为Cu
C.c点溶液中溶质为Zn(NO3)2
D.d点得到的混合物中有2种金属单质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在研究酸和碱的化学性质时,某小组想证明稀硫酸和氢氧化钠混合后,虽然无明显现象,但确实发生了化学反应。试与他们一起完成实验方案的设计、实施和评价,并得出有关结论。
(1)探究稀硫酸和氢氧化钠溶液的反应:
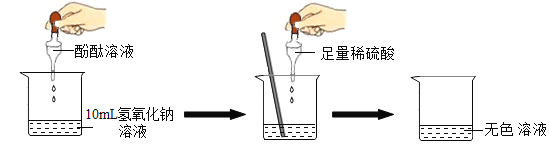
当滴入几滴酚酞溶液后,溶液由无色变为_________色。根据上述实验中颜色变化,可确定稀硫酸和氢氧化钠溶液发生了化学反应。
(2)探究上述稀硫酸和氢氧化钠溶液反应后烧杯中的硫酸是否过量:根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量。同学们又分别选取氯化钡溶液、紫色石蕊溶液设计实验方案,请你判断并(提示:Ba2+与SO42-可形成BaSO4白色沉淀)
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 有白色沉淀生成 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊溶液 | _________ | 稀硫酸过量 |
①上述设计的实验方案中,正确的方案是:__________。
②若请你再设计一个确定稀硫酸是否过量的实验方案,你会选用的药品是_______,实验现象及结论是_____________。
(3)成成同学认为稀硫酸和氢氧化钠溶液的反应没有明显现象,他提出可以对某些有明显现象产生的中和反应进行探究,如稀盐酸和氢氧化铝的反应,可观察到的现象为_________,说明中和反应已经发生,反应的化学方程式为_______________。。(提示:氢氧化铝是不溶于水的白色固体,化学式为Al(OH)3)。
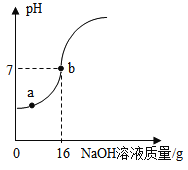
(4)现取10g一定溶质质量分数的稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。计算恰好完全反应时所得溶液的溶质质量分数______。(结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在化学课上,某活动小组将燃烧的钙迅速伸入到盛满CO2的集气瓶中,钙在其中继续燃烧,反应后冷却,瓶底附着一种白色物质。
(提出问题)小组同学一致认为黑色颗粒是单质碳。那么白色物质是什么呢?
(进行猜想)甲同学认为白色物质是氢氧化钙;乙同学认为白色物质可能是CaO;丙同学认为白色物质是CaCO3;丁同学认为白色物质是______________。其他同学立刻认为甲同学的猜想是错误的,理由是_____________。
(实验探究)
实验方案 | 实验操作 | 实验现象 | 结论 |
方案1 | ①取适量白色物质于试管中,加入适量水,振荡,用手触摸试管外壁。 | __________ | 白色物质中含有CaO。丙同学的猜想不正确 |
②静置后,向上层清液中通入二氧化碳。 | _________ | ||
方案2 | 取样品少量于试管中,加入足量稀盐酸,观察现象。 | 没有气泡产生 |
(实验总结)钙在二氧化碳中燃烧的化学方程式为________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年5月18日我国第一艘国产航母试海成功,航母的许多电子元件使用了黄铜。为测定某黄铜(假设合金中仅含铜,锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量(g) | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量(g) | 39.92 | 59.84 | 79.80 | 99.80 |
(1)黄铜粉末完全反应生成氢气的总质量为_______g。
(2)该黄铜中铜的质量分数为多少____________? (写出计算过程)
(3)第三次实验中溶质的种类为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com